
 如果1mol金属R的质量为a g,密度ρ=0.97g•cm-3,请计算出每个R原子的半径的表达式(设钠为紧密堆积结构,见图).
如果1mol金属R的质量为a g,密度ρ=0.97g•cm-3,请计算出每个R原子的半径的表达式(设钠为紧密堆积结构,见图). 分析 由于为紧密堆积的球体,设该晶胞的边长为l,则体积V与密度的关系为4r=$\sqrt{2}$l,得l=2$\sqrt{2}$r,根据ρ=$\frac{m}{V}$来解答.
解答 解:由于为紧密堆积的球体,设该晶胞的边长为l,则体积V与密度的关系为4r=$\sqrt{2}$l,得l=2$\sqrt{2}$r,由均摊法每个晶胞的原子个数为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,根据ρ=$\frac{m}{V}$=$\frac{\frac{4M}{{N}_{A}}}{{l}^{3}}$=$\frac{4M}{(2\sqrt{2}r)^{3}N{\;}_{A}}$=0.97g•cm-3,r3=$\frac{a}{6.02×10{\;}^{23}×4×\sqrt{2}×0.97}$cm3,所以r=$\root{3}{a}$×3.03×10-9cm;
答:原子半径r=$\root{3}{a}$×3.03×10-9cm.
点评 本题考查金属晶体堆积模型,侧重考查学生分析及空间想象能力,注意晶胞中哪些原子紧挨着,为易错点.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:解答题
 某化学课外小组用图装置制取溴苯.
某化学课外小组用图装置制取溴苯. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤⑥ | B. | ②③④⑤ | C. | ①②④⑤⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
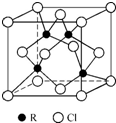 物质的组成、结构都是决定物质性质的重要因素.
物质的组成、结构都是决定物质性质的重要因素. ,其中配体分子中心原子的杂化方式为sp3,与外界离子互为等电子体的一种分子的化学式为SiCl4或SiF4.
,其中配体分子中心原子的杂化方式为sp3,与外界离子互为等电子体的一种分子的化学式为SiCl4或SiF4.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2 | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | 2H2O2═2H2O+O2↑ | D. | 2Al+2NaOH+2H2O═2NaAlO2+3H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com