
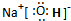 ,所含有的化学键有离子键、共价键;它属于离子化合物(填“离子”或“共价”).
,所含有的化学键有离子键、共价键;它属于离子化合物(填“离子”或“共价”). 分析 X、Y、Z、E、F为五种短周期元素,原子序数依次递增.X+只含有一个质子,则X为H元素;Y的正、负化合价绝对值相等,处于ⅣA族,在同族元素中其氢化物最稳定,则Y为C元素;Z的原子核内质子数是Y的最外层电子数的2倍,则Z的质子数为8,则Z为O元素;F与Z同主族,则F为S元素;E与X同主族,E的原子序数等于O元素,故E为Na元素,据此解答.
解答 解:X、Y、Z、E、F为五种短周期元素,原子序数依次递增.X+只含有一个质子,则X为H元素;Y的正、负化合价绝对值相等,处于ⅣA族,在同族元素中其氢化物最稳定,则Y为C元素;Z的原子核内质子数是Y的最外层电子数的2倍,则Z的质子数为8,则Z为O元素;F与Z同主族,则F为S元素;E与X同主族,E的原子序数等于O元素,故E为Na元素,
(1)由上述分析可知,Y为C元素、Z为O元素、F为S元素,
故答案为:C;O;S;
(2)H、O、Na形成化合物为NaOH,其电子式为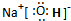 ,所含有的化学键有离子键、共价键,属于离子化合物化合物,
,所含有的化学键有离子键、共价键,属于离子化合物化合物,
故答案为: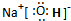 ;离子键、共价键;离子.
;离子键、共价键;离子.
点评 本题考查结构性质位置关系,难度不大,推断元素是解题关键,侧重对基础知识的运用与巩固.


科目:高中化学 来源: 题型:选择题
| A. | A>B>C>D | B. | A>C>D>B | C. | C>A>D>B | D. | C>B>D>A |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸 | H2C2O4 | H2CO3 |
| 电离常数 | K1=5.4×10-2 K2=5.4×10-5 | K1=4.5×10-7 K2=4.7×10-11 |


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
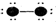
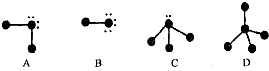
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
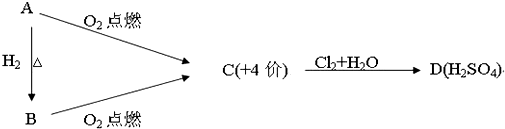
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保护环境:控制“白色污染”--减少和控制使用所有塑料制品防止水的污染--提倡使用无磷洗衣粉 | |
| B. | 基本安全常识:饮用假酒中毒--由甲醇引起食用假盐中毒--由亚硝酸钠引起 | |
| C. | 物质的性质与用途:磺胺类药物能抑制细菌合成核酸--治疗肺炎、脑膜炎、呼吸道感染酸能与碱中和-----胃酸过多的病人服用含氢氧化钠的药物 | |
| D. | 生活中的一些做法:除去衣服上的油污--可用汽油洗涤使煤燃烧更旺--可增大煤与空气接触面积 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
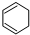 $\stackrel{Br_{2}}{→}$A$→_{△}^{H_{2}/Ni}$B$\stackrel{NaOH溶液}{→}$
$\stackrel{Br_{2}}{→}$A$→_{△}^{H_{2}/Ni}$B$\stackrel{NaOH溶液}{→}$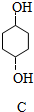 $\stackrel{O_{2}/Cu}{→}$
$\stackrel{O_{2}/Cu}{→}$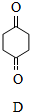
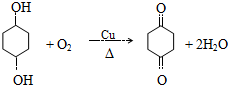 .
.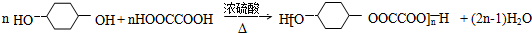 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com