
以下气体发生装置中,不易控制反应产生气体的量的是

 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
使用有机材料制成的塑料薄膜,给环境造成的“白色污染”后果十分严重。我国最近研制成功的一类可降解塑料结构如下,该塑料具有良好的生物适应性和分解性,能自然腐烂分解。试回答下列问题:
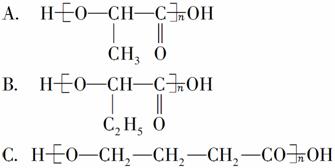
(1)这类可降解塑料中A、B、C的单体分别为________、________、________。
(2)可降解塑料在自然界可通过________(填反应类型)反应分解为小分子有机物。
(3)相同的条件下焚烧下列物质,污染大气最严重的是( )
a.聚氯乙烯 b.可降解塑料
c.聚丙烯 d.有机玻璃
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中各微粒的浓度关系正确的是 ( )
A.室温下,pH=7的醋酸和醋酸钠的混合溶液中:c(CH3COO-)>c(Na+)
B.将10 mL 0.l mol·L-1 Na2CO3溶液逐滴滴加到10 mL 0.l mol·L-1盐酸中:
c(Na+) >c(Cl-) >c(HCO3-) >c(CO32-)
C.等pH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH4+) = c(K+) = c(Ba2+)
D.0.2 mol·L-1的某一元弱酸HA溶液和0.l mol·L-1NaOH溶液等体积混合后的溶液:
2c(OH-) + c(A-) = 2c(H+) + c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物C和E都是医用高分子材料,具有相同的元素百分组成,均可由化合物A制得,如图所示。B和D互为同分异构体。完成下列问题:

(1)化学方程式:A→D______________________________ __________________________________________;
B→C________________________________________________________________________;
(2)反应类型:A→B______________________________ __________________________________________;
B→C________________________________________________________________________;
A→E________________________________________________________________________;
(3)E的结构简式:________________________________ ________________________________________;
(4)A的同系列同分异构体(分子结构中有支链)
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
既能用浓H2SO4干燥,又可用CaO干燥的气体有
①H2 ②O2 ③N2 ④SO2 ⑤H2S ⑥CH4 ⑦NH3 ⑧CO2
A.①②③⑥ B.①②③⑧
C.④⑤⑥ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
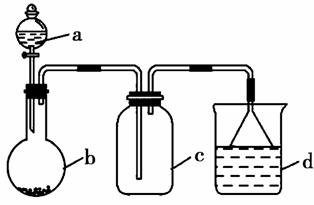
| 选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| C | 稀硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。理论上硫酸和硝酸的物质的量之比最佳为:_________________________________。
(2)实际上,即使铜粉、硫酸及硝酸都比较纯,制得的CuSO4·5H2O中还是有可能存在的杂质是________,除去这种杂质的实验操作称为_____________________________。
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案甲:以空气为氧化剂。将铜粉在________(填仪器名称)中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案乙:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,即发生反应,生成硫酸铜。反应完全后,加物质甲调节pH,铁元素全部沉淀(一般认为铁离子的浓度下降到10-5 mol·L-1,就认为沉淀完全),然后过滤、浓缩、结晶。
请回答下列问题:已知:Ksp[Cu(OH)2]≈10-22,Ksp[Fe(OH)2]≈10-16,Ksp[Fe(OH)3]≈10-38
①为了使铁元素全部沉淀,应调节pH至少为______________________________;
②甲物质可选用的是________;
A.CuCl2 B.NaOH C.Cu2(OH)2CO3 D.CuO E.H2SO4
③反应中加入少量FeSO4对铜的氧化可以起催化作用。其反应过程是:第1步,4Fe2++O2+4H+===4Fe3++2H2O,请写出其第2歩反应的离子方程式_____________________
________________________________________________________________________。
方案丙:将铜丝放到一定量的稀硫酸中,加入适量的H2O2,并控温在50 ℃~60 ℃,持续反应1 h,也能获得硫酸铜。请回答下列问题:
④反应时温度必须控制在50 ℃~60 ℃,温度不宜过高的主要原因是________________________________________________________________________;
⑤写出该反应的化学方程式为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
不饱和酯类化合物在药物、涂料等领域应用广泛。
(1)下列关于化合物Ⅰ的说法,正确的是________。
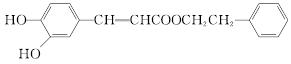
Ⅰ
A.遇FeCl3溶液可能显紫色
B.可发生酯化反应和银镜反应
C.能与溴发生取代反应
D.1 mol 化合物Ⅰ最多能与2 mol NaOH反应
(2)反应①是一种由烯烃直接制备不饱和酯的新方法:
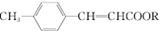
 +2ROH+2CO+O2
+2ROH+2CO+O2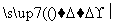 2 +2H2O
2 +2H2O
Ⅱ
化合物Ⅱ的分子式为________,1 mol化合物Ⅱ能与________mol H2恰好完全反应生成饱和烃类化合物。
(3)化合物Ⅱ可由芳香族化合物Ⅲ或Ⅳ分别通过消去反应获得,但只有Ⅲ能与Na反应产生H2。Ⅲ的结构简式为________(写一种);由Ⅳ生成Ⅱ的反应条件为________。
 |
(4)聚合物 可用于制备涂料,其单体结构简式为
________________,利用类似反应①的方法,仅以乙烯为有机物原料合成该单体,涉及的反应方程式为____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
卫生部严令禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。过氧化钙(CaO2)是一种安全无毒物质,带有结晶水,通常还含有CaO。
(1)称取5.42 g过氧化钙样品,灼热时发生如下反应:
2[CaO2·xH2O]―→2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL,该样品中CaO2的物质的量为________。
(2)另取同一样品5.42 g,溶于适量稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀, 得到干燥的CaCO3 7.0 g。
得到干燥的CaCO3 7.0 g。
①样品中CaO的质量为________。
②样品中CaO2·xH2O的x值为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com