
| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 在使酚酞变红的溶液中:Na+、K+、AlO2-、CO32- | |
| C. | 在水电离产生的c(OH-)=1×10-14mol•L-1的溶液中:NH4+、Al3+、SO42-、NO3- | |
| D. | 在pH试纸变深红色的溶液中:K+、Fe2+、Cl-、NO3- |
分析 离子之间能反应生成气体、沉淀、弱电解质或发生氧化还原反应、复分解反应或络合反应的不能大量共存,据此分析解答.
解答 解:A.Fe3+和SCN-发生络合反应生成络合物而不能大量共存,故A错误;
B.能使酚酞试液变红色,说明溶液呈碱性,这几种离子之间不反应且和氢氧根离子不反应,所以能大量共存,故B正确;
C.水电离产生的c(OH-)=1×10-14mol•L-1的溶液呈酸性或碱性,酸性条件下,这几种离子能大量共存,但碱性条件下,NH4+、Al3+不能大量共存,故C错误;
D.pH试纸变深红色的溶液呈强酸性,酸性条件下Fe2+、NO3-发生氧化还原反应而不能大量共存,故D错误;
故选B.
点评 本题考查离子共存,为高频考查,侧重考查复分解反应、氧化还原反应、络合反应,明确离子共存条件及离子性质即可解答,易错选项是C.


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 无法计算 | B. | 6.72L | C. | 33.6L | D. | 22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同温度下两种溶液的pH:Na2CO3>NaHCO3 | |
| B. | 若分别升高温度,两种溶液的pH均减小 | |
| C. | 若分别加入少量NaOH,两溶液中c(CO32-)均增大 | |
| D. | 两溶液中的离子浓度均存在关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Al、Fe、Cu在空气中都易生锈是因为都生成了对应的氧化物 | |
| B. | 在高温下用氢气还原MgCl2可制取金属镁 | |
| C. | 实验测得NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性CH3COOH>H2CO3 | |
| D. | 高温时,CuO比Cu2O稳定,Na2O2比Na2O稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅不与任何酸反应,可用石英制造耐酸容器 | |
| B. | 二氧化氯具有还原性,可用于自来水的杀菌消毒 | |
| C. | 常温下浓硫酸使铝钝化,可在常温下用铝制贮罐贮运浓硫酸 | |
| D. | 二氧化氮溶于水时只生成唯一产物硝酸,工业上利用这一原理生产硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
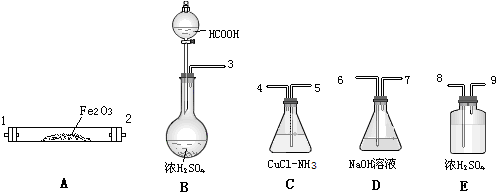
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
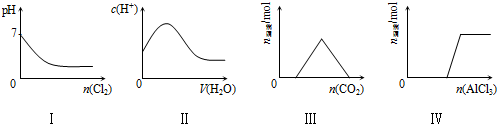
| A. | I表示向Na2SO3溶液中通入Cl2 | |
| B. | II表示向纯CH3COOH中逐滴加水并不断振荡 | |
| C. | III表示向KOH和Ca(OH)2混合液中通入CO2 | |
| D. | Ⅳ表示向NaOH溶液中逐滴加入AlCl3溶液并不断振荡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 277112Cn的原子核内中子数比质子数多53 | |
| B. | Cn元素的相对原子质量为277 | |
| C. | 上述合成过程中属于化学变化 | |
| D. | Cn元素位于元素周期表的第六周期,是副族元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com