
在①KOH、②Al(OH)3、③H2SO4三种物质中,与盐酸和氢氧化钠溶液均能反应的是( )
|
| A. | ①②③ | B. | ②和③ | C. | ①和③ | D. | 只有② |
考点:
两性氧化物和两性氢氧化物.
专题:
元素及其化合物.
分析:
能和盐酸、氢氧化钠溶液反应的物质有:Al、两性氧化物、两性氢氧化物、弱酸的酸式盐、弱酸的铵盐、氨基酸等物质,据此分析解答.
解答:
解:①KOH属于强碱,和盐酸反应生成盐和水,和NaOH溶液不反应,故错误;
②氢氧化铝属于两性氢氧化物,能溶于强酸、强碱,所以能和HCl、NaOH溶液反应生成盐和水,故正确;
③H2SO4属于酸,只能和碱发生中和反应,和酸不反应,所以只和NaOH反应,和HCl不反应,故错误;
故选D.
点评:
本题考查了能和酸、碱反应的物质,明确物质的性质是解本题关键,总结归纳能和强酸、强碱反应的物质,形成知识网络结构,知道常见物质的酸碱性,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
氮的重要化合物如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用.
(1)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体.
①写出该反应的离子方程式:.
②在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝.若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为:;为抑制肼的分解,可采取的合理措施有(任写一种).
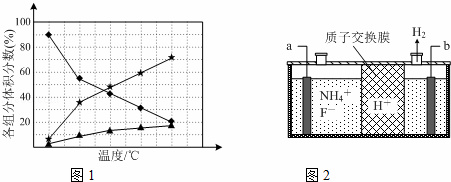
(2)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示.
①氮化硅的化学式为
②a电极为电解池的阳(填“阴”或“阳”)极,写出该电极的电极反应式:电解过程中还会生成少量氧化性极强的气体单质,该气体的分子式是F2.
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下合成乙烯。
6H2(g)+2CO2(g)  C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
 (1)乙烯是___________分子。(填极性或非极性)
(1)乙烯是___________分子。(填极性或非极性)
(2)请在方程式上标出该反应电子转移的方向和数目。
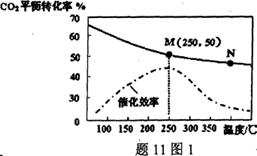
(3)温度对CO2的平衡转化率和催化剂催化效率的影
响如题11图1,下列说法正确的是___________。
A.此反应随温度升高,反应速率一定加快
B.平衡常数:KM>KN
C.M点CO2的平衡转化率受温度、催化剂的共同影响
 (4)若投料比n(H2):n(CO2)=3:1,图中M点乙烯的体积分数为___________ (保留两位有效数字)。
(4)若投料比n(H2):n(CO2)=3:1,图中M点乙烯的体积分数为___________ (保留两位有效数字)。
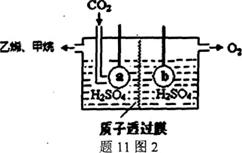
(5)电解法制取乙烯装置如题11图2,电极a接电源的
___________极,生成乙烯的电极反应式为___________。
当左侧有33.6L(标准状况)CO2反应时,左右两侧溶液
质量差|△m右|﹣|△m左|=36g,则乙烯的产率为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列情况可能引起水污染的是( )
①城市污水的任意排放 ②农业生产中农药、化肥使用不当 ③海上石油泄漏 ④工业生产中废液、废气、废渣任意排放.
|
| A. | 只有①③ | B. | 只有①④ | C. | 只有②④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
|
| A. | 钠、钾着火时可用水灭火 |
|
| B. | 面粉厂或加油站不必严禁烟火 |
|
| C. | 氨气泄漏时可喷洒大量水进行处理 |
|
| D. | 节日期间可在人群聚集的闹市燃放烟花爆竹 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子,在指定的环境中可能大量共存的是( )
|
| A. | 水电离出来的c(H+)=10﹣13mol/L的溶液:K+、HCO3﹣、Br﹣、Ba2+ |
|
| B. | 滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl﹣、NO3﹣ |
|
| C. | 与金属铝反应只能放出氢气的溶液:NO3﹣、K+、Cl﹣、Na+、OH﹣ |
|
| D. | c(H+)>c(OH﹣)的溶液中:Na+、K+、SO42﹣、S2﹣ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com