
空气吹出法是最早工业化海水提溴的方法,适合从低浓度含溴溶液中提取溴。
 |
(1)NaBr的电子式是 。
(2)反应①是将Br—转化为Br2,反应①的离子方程式是 。
(3)通入空气吹出Br2,并用Na2CO3吸收的目的是 。
(4)反应②的化学方程式是 。
(5)反应③中每生成3 mol Br2,转移电子的物质的量是 mol。
(6)为了除去工业Br2中微量的Cl2,可向工业Br2中 (填字母)。
a.通入HBr b.加入NaBr溶液 c.加入Na2CO3溶液 d.加入Na2SO3溶液
答案: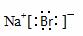
(1) (2)Cl2+2Br— Br2+2Cl—(物质1分,配平1分)
Br2+2Cl—(物质1分,配平1分)
(3)富集溴
(4)3Br2+3Na2CO3 5NaBr+3CO2+NaBrO3 (物质1分,配平1分)
5NaBr+3CO2+NaBrO3 (物质1分,配平1分)
(5)5 (6)b
解析:分析流程知,浓缩的海水中有低浓度的溴离子,在酸性环境中,加入氯气,发生氧化还原反应:Cl2+2Br-=2Cl-+Br2,得到低浓度Br2溶液,通入空气吹出Br2,Br2与Na2CO3发生反应:3Br2+3Na2CO3 5NaBr+3CO2+NaBrO3,然后将产物溶于水,酸化,有归中反应:5Br-+6H++BrO3-
5NaBr+3CO2+NaBrO3,然后将产物溶于水,酸化,有归中反应:5Br-+6H++BrO3- 3Br2+3H2O,此步骤能将Br2富集。根据电子转移守恒,计算得出若生成生成3 mol Br2,转移电子的物质的量是5mol。要除去工业Br2中微量的Cl2,选择的试剂最好能将Cl2转化成Br2,且反应所得物质较易分离。且不产生新的杂质,综合分析只有b合题意。
3Br2+3H2O,此步骤能将Br2富集。根据电子转移守恒,计算得出若生成生成3 mol Br2,转移电子的物质的量是5mol。要除去工业Br2中微量的Cl2,选择的试剂最好能将Cl2转化成Br2,且反应所得物质较易分离。且不产生新的杂质,综合分析只有b合题意。


 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
某无色溶液,其中可能存在的离子有:Na+、Ag+、Ba2+、Fe3+、Al3+、AlO2-、
S2-、SO32-、CO32-、SO42-,现取该溶液进行实验,实验结果如下:
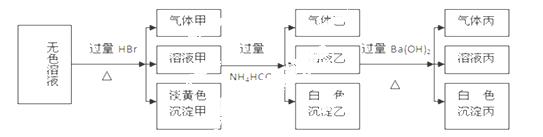
试回答下列问题:
(1)生成沉淀甲的离子方程式为: 。
(2)由溶液甲生成沉淀乙的离子方程式为 。
(3)已知气体甲由两种氧化物组成(不包括水蒸汽和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入下表(表中每一行对应正确即可得分)
| 步骤 | 实验目的 | 试剂 | 现象 |
| 1 | |||
| 2 | |||
| 3 | 检验CO2 | 澄清石灰水 | 溶液变浑浊 |
(4)综上所述,该溶液肯定存在的离子有: 。
(5)针对溶液中可能存在的离子,用实验证明是否存在的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C三种气体,A是密度最小的气体,B在通常情况下呈黄绿色,纯净的A可以在B中安静地燃烧生成C。把气体B通入到适量石灰乳中可以得到白色浑浊物D。请据此回答下列问题:
(1)写出下列各反应的化学方程式。
①纯净的A在B中安静地燃烧生成C:__________________________;
②将气体B通入到水中:_______________________________________;
③将气体B通入到NaOH溶液中:______________________________;
④将气体B通入到适量石灰乳中:________________________________。
(2)把三种气体分别通入酸性硝酸银溶液中,出现白色沉淀的气体是:________(用字母表示)。
(3)白色浑浊物D因具有漂白性又称为________,该物质在空气中容易变质的原因为(用化学方程式表示)________________ ___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中的杂质选用的试剂和方法最合理的是
| 物质 | 杂质 | 试剂 | 方法 | |
| A | 甲烷 | 乙烯 | 酸性高锰酸钾溶液 | 洗气 |
| B | 氯化亚铁溶液 | 氯化铁 | 过量铁粉 | 过滤 |
| C | 二氧化硅 | 氧化铝 | 氢氧化钠溶液 | 过滤 |
| D | 乙酸乙酯 | 乙酸 | 饱和碳酸钠溶液 | 蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列四种元素中,第一电离能由大到小顺序正确的是
①.原子含有未成对电子最多的第二周期元素
②.电子排布为1s2的元素
③.周期表中电负性最强的元素
④.原子最外层电子排布为3s23p4的元素
A.②③①④ B.③①④② C.①③④② D.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
如图利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )
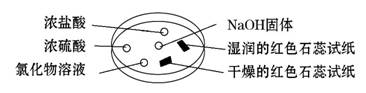
| 选项 | 实验现象 | 解释 |
| A | 浓盐酸附近产生白烟 | NH3与浓盐酸反应生成了NH4Cl固体 |
| B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
| C | 氯化物溶液变浑浊 | 该溶液一定是AlCl3溶液 |
| D | 干燥的红色石蕊试纸不变色,湿润的红色石蕊试纸变蓝 | NH3是一种可溶性碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知101KPa时辛烷的标准燃烧热为—5518kJ·mol-1,含20gNaOH的稀溶液与稀盐酸充分反应放出热量28.7kJ,则下列热化学方程式书写正确的是
①C8H18(l)+ 25/2O2(g)= 8CO2(g)+ 9H2O(g); △H = +5518 kJ·mol-1
②C8H18(l)+ 25/2O2(g)= 8CO2(g)+ 9H2O(l); △H = -5518 kJ·mol-1
③H+(aq)+ OH-(aq)= H2O(l); △H = -57.4 kJ·mol-1
④HCl (aq) + NaOH(aq) =NaCl(aq) + H2O(l); △H = —28.7 kJ·mol-1
A.①③ B.②③ C.②④ D.②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com