
| A�� | 22.4LCH4��CH3Cl�Ļ���������еķ�����ĿΪNA | |
| B�� | 1mol������������й��õ��Ӷ���Ϊ3NA | |
| C�� | �ö��Ե缫���1 LŨ�Ⱦ�Ϊ2 mol/L��AgNO3��Cu��NO3��2�Ļ����Һ������0.2 NA������ת��ʱ����������6.4g���� | |
| D�� | 0.1mol Na2CO3•10H2O�ھ����л���Һ�У����е�CO32-���Ӿ�С��0.1 NA |
���� A���������������������֪����Vm����ֵ��֪�������㣻
B����������ĵ���ʽΪ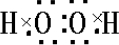 ���ɵ���ʽ���жϹ��õ��Ӷ�����
���ɵ���ʽ���жϹ��õ��Ӷ�����
C��Ag+�����Դ���Cu2+�����������ӵķŵ�˳���жϣ�
D���ھ�����CO32-������ˮ�⣬����Һ�з���ˮ�⣮
��� �⣺A��Vm���¶Ⱥ�ѹǿ��Ӱ�죬�¶Ⱥ�ѹǿ��֪����Vm����ֵ��֪�����������ʵ���������������A����
B����������ĵ���ʽΪ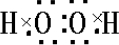 ���ɵ���ʽ��֪��1mol������������й��õ��Ӷ���Ϊ3NA����B��ȷ��
���ɵ���ʽ��֪��1mol������������й��õ��Ӷ���Ϊ3NA����B��ȷ��
C��Ag+�����Դ���Cu2+��1LŨ�Ⱦ�Ϊ2mol/L��AgNO3��Cu��NO3��2�Ļ����Һ������0.2mol����ת��ʱ����������Ag������Ϊ0.2mol��108g/mol=21.6g����C����
D���ھ�����CO32-������ˮ�⣬����Һ�з���ˮ�⣬��˾�����CO32-������Ϊ0.1 NA����Һ��CO32-����С��0.1 NA����D����
��ѡB��
���� ���⿼�鰢��٤�������ļ������жϣ���Ŀ�Ѷ��еȣ��漰֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ���ѧ���ķ������������������Ӧ�û���֪ʶ��������ע��ŵ�˳���ˮ�ⷢ����������


 ���Ǽ���С����ϵ�д�
���Ǽ���С����ϵ�д� �Ͻ�ƽ���Ȿϵ�д�
�Ͻ�ƽ���Ȿϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
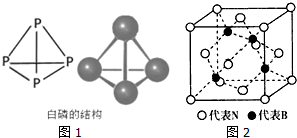 �������ڱ���ͬ��Ԫ�ص������ԣ���Ԥ��Ԫ�ص����ʣ�
�������ڱ���ͬ��Ԫ�ص������ԣ���Ԥ��Ԫ�ص����ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȳ | B�� | �� | ||
| C�� | һ����ϩ��CH2=CHCl�� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
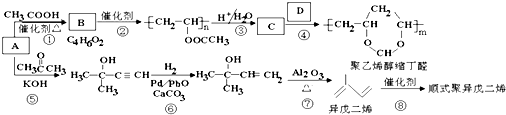
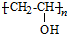 ��CH3CH2CH2CHO��
��CH3CH2CH2CHO��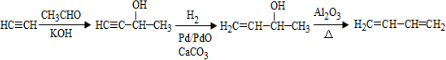 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ƶ���ˮ�ڹ�������ɫ��dz | |
| B�� | ������������������ɺ��ɫ���� | |
| C�� | �ںϳɰ��ķ�Ӧ�У����»��ѹ�����ڰ��ĺϳ� | |
| D�� | Fe��SCN��3��Һ�м���6mol/L NaOH��Һ����ɫ��dz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢޢߢ� | B�� | �ۢܢݢ� | C�� | �ۢܢޢ� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Mg��Al | B�� | Mg��Zn | C�� | Al��Zn | D�� | Al��Fe |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
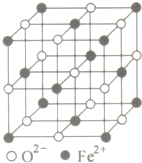 ��Щʳ������Ԫ�غ����dz��ḻ�����з�Ѫ������������ڵ���ʽ֮һ����Ҫ���������뵰���ʺ������ϳ�����
��Щʳ������Ԫ�غ����dz��ḻ�����з�Ѫ������������ڵ���ʽ֮һ����Ҫ���������뵰���ʺ������ϳ������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com