
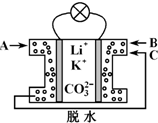
 熔融碳酸盐燃料电池是一种高温电池,具有效率高、噪音低、无污染、燃料多样化、余热利用价值高和电池构造材料价廉等诸多优点,是未来的绿色电站.某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见下图.下列说法正确的是( )
熔融碳酸盐燃料电池是一种高温电池,具有效率高、噪音低、无污染、燃料多样化、余热利用价值高和电池构造材料价廉等诸多优点,是未来的绿色电站.某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见下图.下列说法正确的是( )| A. | Li+、K+移向左侧电极 | |
| B. | 外电路中电子由右侧电极移向左侧电极 | |
| C. | 通入1 mol气体A时,左侧电极上生成5 mol CO2 | |
| D. | 相同条件下通入气体B与气体C的体积比为2:1 |
分析 该原电池为甲烷燃料电池,通入燃料的电极为负极、通入氧化剂的电极为正极,负极反应式为CH4+4CO32--8e-=5CO2+2H2O,正极反应式为O2+2CO2+4e-═2CO32-,据原电池的工作原理分析解答.
解答 解:该原电池为甲烷燃料电池,通入燃料的电极为负极、通入氧化剂的电极为正极,负极反应式为CH4+4CO32--8e-=5CO2+2H2O,正极反应式为O2+2CO2+4e-═2CO32-,负极上产生的二氧化碳可以为正极所利用,所以A是负极,B是正极.
A、燃料电池中通入燃料的电极是负极、通入氧化剂的电极是正极,原电池放电时,阳离子向正极移动,Li+、K+移向右侧电极移动,故A错误;
B、外电路中电子由负极流向正极,即从左侧电极移向右侧电极,故B错误;
C、负极反应式为CH4+4CO32--8e-=5CO2+2H2O,正极反应式为O2+2CO2+4e-═2CO32-,通入1mol气体甲烷气时,左侧电极上生成5 molCO2,故C正确;
D、相同条件下通入气体B与气体C的体积比为1:2,故D错误.
故选C.
点评 本题考查了化学电源新型电池,明确原电池中物质得失电子、电子流向、离子流向即可解答,难点是电极反应式书写,要根据电解质确定正负极产物,难度中等.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙醇的分子式:CH3CH2OH | B. | CH3COCH3的官能团名称:醚键 | ||
| C. | 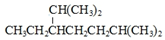 的名称为:2,6-二甲基-3-乙基庚烷 的名称为:2,6-二甲基-3-乙基庚烷 | D. | 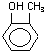 的类别:醇类 的类别:醇类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{34}^{78}$Se与${\;}_{34}^{80}$Se都含有34个中子 | |
| B. | ${\;}_{34}^{78}$Se与${\;}_{34}^{80}$Se分别含有44和46个质子 | |
| C. | ${\;}_{34}^{78}$Se与${\;}_{34}^{80}$Se因含有相同的质子数故互为同位素 | |
| D. | ${\;}_{34}^{78}$Se与${\;}_{34}^{80}$Se含有相同的电子数,因此性质一样 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸馏水润湿的试纸测某溶液的pH,一定会使结果偏低 | |
| B. | 蒸馏操作时,冷却水应从冷凝管的下口通入,上口流出 | |
| C. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| D. | 蒸发操作时,当有较多晶体析出时,停止加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
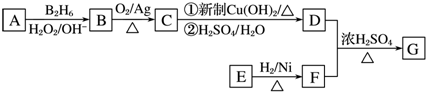
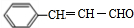 ;
;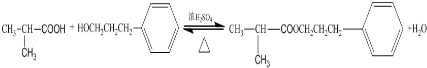 ;
;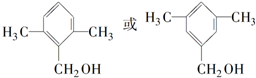 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对“地沟油”进行分馏可得到汽油 | |
| B. | PM2.5、CO2都属于空气质量日报的内容 | |
| C. | 硅酸多孔、吸水能力强,常用作袋装食品的干燥 | |
| D. | 向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,1 mol•L-1甲酸溶液的pH值约为2 | |
| B. | 甲酸电离出的阳离子全部是H+ | |
| C. | 10mL1 mol•L-1甲酸与10 mL1 mol•L-1NaOH溶液完全反应后,溶液呈碱性 | |
| D. | 1LH+浓度为0.1 mol•L-1的甲酸和足量Zn反应放出的H2在标况下远大于1.12L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 硅酸盐工业使用的每一种原料中都含有硅元素 | |
| B. | 水泥.普通玻璃都是混合物 | |
| C. | 生产水泥和玻璃都需用石灰石 | |
| D. | 用纯净的石英可制成石英玻璃,它的膨胀系数小,常用来制造耐高温的化学仪器 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
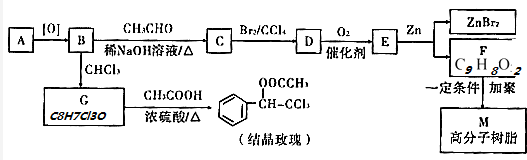
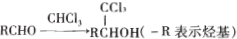
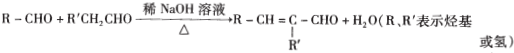
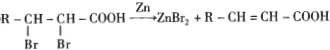
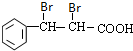 .
.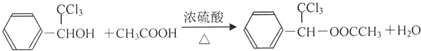 .
.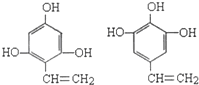 .
.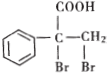 是一种重要的药物中间体,其合成路线与E相似,请以
是一种重要的药物中间体,其合成路线与E相似,请以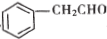 为原料设计它的合成路线(其他所需原料自选).
为原料设计它的合成路线(其他所需原料自选).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com