
分析 室温下单质A与某种常见一元强碱溶液反应,可得到B和C,且A、B、C中都含有X,说明A中元素在碱中发生了歧化反应,常温下能与碱溶液发生歧化反应的在中学化学中主要是Cl2、Br2等,一定条件下化合物D受热分解生成B,可制得元素Y的单质,可知应为KClO3分解,由此可知X为氯元素,Y为氧元素,Z为K元素,A为Cl2,D为KClO3,B为KCl,C为KClO,验证符合,据此解答.
解答 解:室温下单质A与某种常见一元强碱溶液反应,可得到B和C,且A、B、C中都含有X,说明A中元素在碱中发生了歧化反应,常温下能与碱溶液发生歧化反应的在中学化学中主要是Cl2、Br2等,一定条件下化合物D受热分解生成B,可制得元素Y的单质,可知应为KClO3分解,由此可知X为氯元素,Y为氧元素,Z为K元素,A为Cl2,D为KClO3,B为KCl,C为KClO,验证符合,
(1)X为氯元素,Y为氧元素,Z为K元素,故答案为:Cl;K;
(2)③中氯气与氢氧化钾反应,生成氯化钾、次氯酸钾和水,反应的化学方程式为:Cl2+2KOH=KCl+KClO+H2O,
故答案为:Cl2+2KOH=KCl+KClO+H2O;
(3)④中氯酸钾分解生成氯化钾和氧气,反应方程式为2KClO3$\frac{\underline{\;二氧化锰\;}}{△}$2KCl+3O2↑,故答案为:2KClO3$\frac{\underline{\;二氧化锰\;}}{△}$2KCl+3O2↑.
点评 本题考查元素化合物推断,需要学生熟练掌握元素化合物性质,综合题中信息,进行猜测,再顺推、逆推和逐个验证,难度中等.


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:解答题
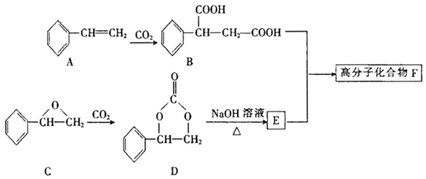
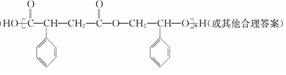
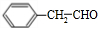 ,G与新制的Cu(OH)2悬浊液混合加热时发生反应的化学方程式为
,G与新制的Cu(OH)2悬浊液混合加热时发生反应的化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 | |
| B. | IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 | |
| C. | 氯最高价氧化物对应的水化物为HClO4;则氟最高价氧化物对应的水化物HFO4 | |
| D. | NaHSO4与NaHSO3溶于水显酸性,由所有酸式盐溶于水显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 碳 | 氮 | Y | |
| X | 硫 | Z |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④ | C. | ③④ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
| 920℃ | 97.8℃ | 1 291℃ | 190℃ | 2 073℃ | -107℃ | -57℃ | 1 723℃ |
| A. | 只要由金属元素和非金属元素形成的晶体就一定是离子晶体 | |
| B. | 在共价化合物分子中各原子都形成8个电子的稳定结构 | |
| C. | 金属晶体的熔点不一定比分子晶体的高 | |
| D. | 同族元素的氧化物不可能形成不同类型的晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com