
下列图示与对应的叙述相符的是

A.图1表示0.001 mol·L一1盐酸滴定0.001 mol·L一1NaOH溶液的滴定曲线
B.图2所示,石墨的熔点比金刚石低
C.图3表示的是Al3+与OH一反应时含铝微粒浓度变化曲线,图中a区域的物质是Al(OH)3
D.图4所示,图中的阴影部分面积的含义是「v(正)一v(逆)〕
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源:2015-2016学年四川省高一上第三次月考化学试卷(解析版) 题型:选择题
近年来,光化学烟雾污染问题已引起人们的注意,下列哪种气体是造成光化学烟雾的主要因素
A.NO2 B.SO2 C.CO2 D.Cl2
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
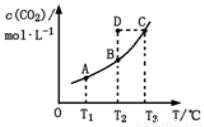
A. 反应CO(g)+H2O(g) CO2(g)+H2(g)的 ΔH>0
CO2(g)+H2(g)的 ΔH>0
B. 在T2时,若反应处于状态D,则一定有ν正<ν逆
在T2时,若反应处于状态D,则一定有ν正<ν逆
C. 平衡状态A与C相比,平衡状态A的c(CO)小
D. 若T1、T2时的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.盐酸中滴加氨水至中性,溶液中溶质为氯化铵
B.稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小
C.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH值不变
D.沸水中滴加适量饱和FeCl3溶液,形成带电的 胶体,导电能力增强
胶体,导电能力增强
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期12月统考化学试卷(解析版) 题型:实验题
已知磺酰氯(SO2Cl2)是一种有机氯化物,也是锂电池正极活性物质,SO2Cl2是一种无色液体,熔点—54.1 ℃,沸点69.1 ℃,极易水解,遇潮湿空气会产生白雾。磺酰氯(SO2Cl2)的制备方法及装置图如下:SO2(g)+Cl2(g) SO2C12(g)
SO2C12(g)  H<0,
H<0,
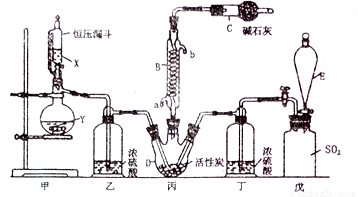
(1)化合物SO2Cl2中S元素的化合价是 。
(2)仪器D的名称是 ,仪器C的作用除了吸收氯气和二氧化硫,还具有 作用。
(3)戊是贮气装置,则E中的溶液是 ;若缺少装置乙和丁,则产物变质,发生反应的化学方程式是
(4)反应结束后,将丙中混合物分离开的实验操作是 。
(5)有关该实验叙述正确的是
a、X、Y最好的席间组合是铜片和浓硫酸
b、活性炭的作用是作催化剂
c、冷凝管B也可以用作蒸馏
(6)GET公司开发的Li-SO2Cl2军用电池,其示意图如图所示,已知电池反应为: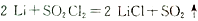 ,则电池工作时,正极的电极反应式为是
,则电池工作时,正极的电极反应式为是

查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期12月统考化学试卷(解析版) 题型:选择题
在一定温度下,可逆反应A(g) +3B(g)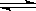 2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
A.A,B,C的分子数之比为1:3:2
B.C生成速率与A生成速率相等
C.单位时间内生成n molA同时3n mo1B
D.A,B、C的浓度不再变化
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上学期第二次精英对抗赛化学试卷(解析版) 题型:填空题
二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用下图所示的装置模拟制取并收集ClO2。
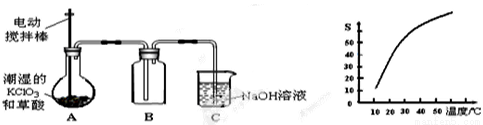
(1)B必须放在冰水浴中控制温度,其原因是 。
(2)反应后在装置C中可得NaClO2溶液。已知NaClO2饱和溶液中在温度低于38℃时析出晶体是NaClO2·3H2O,在温度高于38℃时析出晶体是NaClO2。根据右上图所示的NaClO2溶解度曲线,请补充从NaClO2溶液中制NaClO2操作步骤:a ;b ;③洗涤;④干燥。
(3)亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。

① Ⅱ中反应的离子方程式是 。
② ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备。写出该反应化学方程式 。
③ NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+物质的量 。(填“相同”,“不同”或“无法判断”)
查看答案和解析>>
科目:高中化学 来源:2016届湖南省郴州市高三上学期12月教学质量监测理综化学试卷(解析版) 题型:填空题
某硅铁矿中主要含Si02、Fe304、Al203、Cu0。某工厂用它为原料进行综合应用来制取硅胶、铁红、铝、胆矾晶体,设计如下工业流程图:
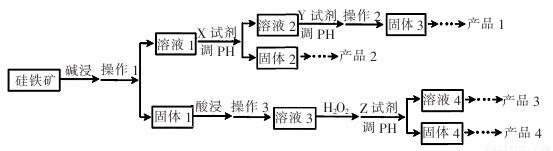
已知:Fe(OH)2、Fe(OH)3、Cu(OH)2完全沉淀的PH分别为9.6、3.7、9.4。
(1)碱浸时发生的离子反应方程式为:_
(2)为提高碱浸的浸出率,可采取的方法有 。(填两种即可)
(3)溶液3中加H2O2的目的是 。 对应的离子反应方程式为:________。
(4)Z试剂可以选用下列的 (填字母)
a. Cu b.CuO c.Cu(OH)2 d.CuCO3
(5)由溶液4制取产品3还要先加热到____(填字母)时,停止加热、冷却结晶。
A.沸腾
B.液体表面出现晶膜
C.析出大量晶体
D.快蒸干,还有少量液体
(6)判断固体4对应的元素沉淀完全的方法是:________________。
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上学期第二次精英对抗赛化学试卷(解析版) 题型:选择题
在一种酸性溶液中存在NO3-、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,由此可推知该溶液中
A.一定含有I-,不能确定是否含有Cl-
B.一定含有NO3-
C.不含有Fe3+,可能含有NO3-
D.一定含有I-、NO3-和Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com