
短周期主族元素A、B、C、D、E的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,E原子最外层电子数是B原子内层电子数的3倍或者C原子最外层电子数的3倍,B、D原子最外层电子数之和等于C、E原子最外层电子数之和。下列说法正确的是
A.元素B和E的氧化物对应的水化物均为强酸
B.C的单质能与A的氧化物发生置换反应
C.元素C、D、E的最高价氧化物对应的水化物之间均可相互反应
D.工业上常用电解元素C、D的氯化物来制取它们的单质
B
解析试题分析:E原子最外层电子数是B原子内层电子数的3倍或者C原子最外层电子数的3倍,说明E元素最外层电子数为6,则C最外层电子数为2。B、C、E原子的最外层电子数之和为13,说明B元素最外层电子数为13-6-2=5,因此B元素的核外电子数为2+5=7,为N元素。E的原子序数最大,应为S元素,则C应为Mg元素。B、D原子最外层电子数之和等于C、E原子最外层电子数之和,即2+6=8,因此D的最外层电子数为8-5=3,应为Al元素,A、B两元素相邻,则A应为C元素,B为N元素,C为Mg元素,D为Al元素,E为S元素。A、B为氮元素,氧化物对应水化物是硝酸和亚硝酸,亚硝酸是弱酸。E为S元素,氧化物对应的水化物分别为H2SO3和H2SO4,其中H2SO3为弱酸,故A错误;B、Mg在CO2中燃烧,反应生成C和MgO,为置换反应,故B正确;C、元素C、D、E的最高价氧化物对应的水化物分别为Mg(OH)2、Al(OH)3、H2SO4,其中Mg(OH)2和Al(OH)3不反应,故C错误;D.AlCl3为共价化合物,熔融状态下不导电,工业用电解Al2O3的方法冶炼铝,故D错误,答案选B。
考点:考查位置、结构、性质关系的有关判断


科目:高中化学 来源: 题型:单选题
门捷列夫在研究周期表时预言了包括“类铝”、“类硅”在内的11种元素。
(1)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(Ge)。
①已知主族元素锗的最高化合价为+4价,其最高价氧化物的水化物为两性氢氧化物。试比较元素的非金属性Si________Ge(用“>”或“<”表示)。
②若锗位于硅的下一周期,写出“锗”在周期表中的位置________。根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是________。
③硅和锗单质分别与H2反应时,反应较难进行的是________(填“硅”或“锗”)。
(2)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
①由镓的性质推知,镓与铝同主族,且位于铝的下一周期。试从原子结构的角度解释镓与铝性质相似的原因________________。冶炼金属镓通常采用的方法是________________。
②为判断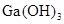 是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、________和________。
是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、________和________。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关原子结构和元素周期律的表述中不正确的是( )
①原子序数为l5的元素的氢化物为三角锥形
②ⅦA族元素是同周期中非金属性最强的元素
③第三周期ⅣA族元素的原子核电荷数和中子数均为6
④原子序数为26的元素位元素周期表的的第四周期第族
A.①② B.①③ C②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z在元素周期表中的位置如图所示。下列说法正确的是
| A.原子半径的大小为:Z>Y>X |
| B.若X的一种单质为原子晶体,则含Y元素的盐溶液一定呈酸性 |
| C.若Y可作半导体材料,则X、Z的单质均为分子晶体 |
| D.若Y与Z的核电荷数之和为X的4倍,则X、Z各自形成的氢化物熔沸点:X<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
镭是元素周期表中第7周期第IIA族元素,下列有关叙述不正确的是
| A.镭的金属性比钙弱 | B.单质能与水反应生成H2 |
| C.镭在化合物中呈+2价 | D.碳酸镭难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液。下列说法不正确的是
| A.离子半径的大小顺序为W>Q>Z>X>Y |
| B.元素X的气态氢化物与Q的单质可发生置换反应 |
| C.元素X与Y可以形成5种以上的化合物 |
| D.元素Z、W、Q的单质在一定条件下均能和强碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
现有三种元素的基态原子的电子排布式如下:① 1s22s22p63s23p1;②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.电负性:①>②>③ | D.最高正化合价:③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素W、X、Y和Z的原子序数依次增大,元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是
| A.元素W、X的氯化物中,各微粒均满足8电子的稳定结构 |
| B.元素X与氢形成的电子比为1:1的化合物有很多种 |
| C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 |
| D.元素Z可与元素X形成共价化合物XZ2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com