
已知MgO、MgCl2的熔点分别为2800℃、604℃,将MgO、MgCl2加热熔融后通电电解,都可得到金属镁。海水中含有MgCl2,工业上从海水中提取镁,正确的方法是( )
A. 海水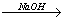 Mg(OH)2
Mg(OH)2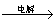 Mg
Mg
B. 海水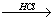 MgCl2溶液
MgCl2溶液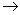 MgCl2熔融
MgCl2熔融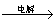 Mg
Mg
C. 海水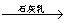 Mg(OH)2
Mg(OH)2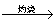 MgO
MgO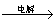 Mg
Mg
D.海水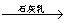 Mg(OH)2
Mg(OH)2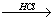 MgCl2溶液
MgCl2溶液 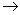 MgCl2熔融
MgCl2熔融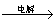 Mg
Mg
科目:高中化学 来源: 题型:
下列叙述中,正确的是( )
A.石油、煤、天然气、氢气都属于化石燃料
B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH<0
C.人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,某物质的热值越高则其标准燃烧热越大
D.两个体积相同的容器中充入等量的NO2发生反应:2NO2(g)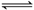
 N2O4(g) ΔH<0,绝热容器中气体的颜色比恒温容器中颜色深
N2O4(g) ΔH<0,绝热容器中气体的颜色比恒温容器中颜色深
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关离子晶体的数据大小比较不正确的是( )。
A.熔点:NaF>MgF2>AlF3
B.晶格能:NaF>NaCl>NaBr
C.阴离子的配位数:CsCl>NaCl>CaF2
D.硬度:MgO>CaO>BaO
查看答案和解析>>
科目:高中化学 来源: 题型:
在2 L容积不变的容器中,发生N2+3H2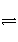
 2NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol/(L·s),则10 s后容器中N2的物质的量是( )
2NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol/(L·s),则10 s后容器中N2的物质的量是( )
A.1.6 mol B.2.8 mol C.3.2 mol D.3.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ,某有机物分解的反应可表示为:
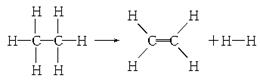
若在反应中消耗了1 mol乙烷,则有关该反应的说法正确的是( )
A.该反应放出251.2 kJ的热量 B.该反应吸收251.2 kJ的热量
C.该反应放出125.6 kJ的热量 D.该反应吸收125.6 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
在200℃时,将a mol H2(g)和b mol I2(g)充入到体积为V L的密闭容器中,发生反应:I2(g)+H2(g)⇋2HI(g)。
(1)反应刚开始时,由于c(H2)=_______,c(I2)=_______,而c(HI)=________,所以化学反应速率________最大而________最小(为零)(填“v正”或“v逆”)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)________,c(I2)________,而c(HI)________,从而化学反应速率v正________,而v逆________(填“增大”、“减小”或“不变”)。
(3)当反应进行到v正与v逆________时,此可逆反应就达到了最大限度,若保持外界条件不变时,混合物中各组分的物质的量、物质的量浓度、质量分数、体积分数、反应物的转化率和生成物的产率及体系的总压强(或各组分的分压)都将________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应方程式中有一个与其他三个在分类上不同,这个反应是( )
A.S+O2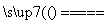 SO2 B.Na2CO3+CO2+H2O===2NaHCO3
SO2 B.Na2CO3+CO2+H2O===2NaHCO3
C.NH4HCO3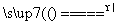 NH3↑+CO2↑+H2O D.CO2+C
NH3↑+CO2↑+H2O D.CO2+C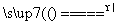 2CO
2CO
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-===Cl2↑
B.氢氧燃料电池的负极反应式为:O2+2H2O+4e-===4OH-
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-===Cu2+
D.钢铁发生电化学腐蚀的正极反应式为:Fe-2e-===Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于溶液的酸碱性,说法正确的是( )
A.pH=7的溶液呈中性
B.中性溶液中一定有[H+]=1.0×10-7 mol·L-1
C.[H+]=[OH-]的溶液呈中性
D.在100℃时,纯水的pH<7,因此显酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com