
| A、雾属于胶体,能产生丁达尔现象 |
| B、目前的雾霾污染,无需治理借助于天气状况改善即可 |
| C、PM2.5颗粒含有重金属、多种烃等有毒物质 |
| D、汽车尾气是目前城市大气污染气体和细小颗粒物产生的一个重要来源 |


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
| A、氢键属于共价键 |
B、因为分子间存在氢键的缘故, 比 比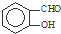 熔沸点高 熔沸点高 |
| C、由于氢键比范德华力强,所以H2O分子比H2S分子稳定 |
| D、1mol冰中有4mol氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向氯化铝溶液中加入过量的氨水:3NH3?H2O+A13+═3NH4++Al(OH)3↓ |
| B、NaOH溶液吸收少量CO2:OH-+CO2═HCO3- |
| C、向氯化铁溶液中加入铜粉发生的反应:Cu+Fe3+═Cu2++Fe2+ |
| D、Na2O2与水的反应:Na2O2+H2O═2Na++2OH-+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com