
可逆反应aA(g)+bB(g) 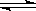 cC(g)+dD(g) ΔH,同时符合下列两图中各曲线的是( )
cC(g)+dD(g) ΔH,同时符合下列两图中各曲线的是( )
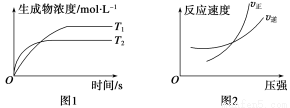
A.a+b>c+d,T1<T2,ΔH<0 B.a+b>c+d,T1>T2,ΔH>0
C.a+b<c+d,T1>T2,ΔH>0 D.a+b<c+d,T1<T2,ΔH<0
科目:高中化学 来源:2016-2017学年江西省高二上期中理化学卷(解析版) 题型:填空题
在25℃时,对于0.1mol·L-1的氨水,请回答以下问题。
(1)若向氨水中加入少量硫酸铵固体,此时溶液中 将_________(填“增大”、“减小”或“不变”);
将_________(填“增大”、“减小”或“不变”);
(2)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,此时溶液的pH_________7(填“>”、“<”或“=”),用离子方程式表示其原因______________,此时溶液中各离子浓度由大到小的顺序为_______________。
(3)若向氨水中加入0.05mol•L-1稀硫酸至溶液正好呈中性,所用氨水的体积V1与稀硫酸的体积V2的关系为V1_________V2(填“大于”、“小于”或“等于”),写出溶液中各离子浓度之间满足的电荷守恒表达式______________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团二师华山中学高一期中化学卷(解析版) 题型:实验题
用Na2CO3·10H2O晶体,配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1) 应称取Na2CO3·10H2O晶体的质量: 。
(2) 根据下列操 作对所配溶液的浓度产生的影响,完成下列要求:
作对所配溶液的浓度产生的影响,完成下列要求:
① Na2CO3·10H2O晶体失去了部分结晶水
② 用“左码右物”的称量方法称量晶体(使用游码)
③ 碳酸钠晶体不纯,其中混有氯化钠
④ 称量碳酸钠晶体时所用砝码生锈
⑤ 容量瓶未经干燥使用
⑥ 定容时俯视容量瓶刻度线
其中引起所配溶液浓度偏高的有 (填序号,下同),偏低的有 ,无影响的有 。
(3)下列操作中,容量瓶所不具备的功能有 。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团二师华山中学高一期中化学卷(解析版) 题型:选择题
下列关于胶体和溶液的说法中正确的是
A.胶体不均一、不稳定,静置后易产生沉淀,溶液均一、稳定、静置不产生沉淀
B.溶液和胶体都是纯净物,浊液是混合物
C.光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应
D.只有胶状物如胶水、果冻类的物质才能称为胶体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团二师华山中学高二期中化学卷(解析版) 题型:填空题
对于A+2B(气) nC(气)在一定条件下达到平衡后,改变下列条件,请回答:
nC(气)在一定条件下达到平衡后,改变下列条件,请回答:
(1)A量的增加或减少,平衡不移动,则A为_________态。
(2)增压,平衡不移动,当n=2时,A的状态为___________;当n=3时,A的状态为_________。
(3)若A为固体,增大压强,C的组分含量减少,则n的取值范围___________。
(4)升温,平衡向右移动,则该反应的逆反应为___________反应。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团二师华山中学高二期中化学卷(解析版) 题型:选择题
在可逆反应中,改变下列条件一定能加快反应速率的是( )
A.增大反应物的量 B.升高温度 C.增大压强 D.使用催化剂
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上学期月考二化学卷(解析版) 题型:填空题
(12分)
Ⅰ.某温度下,0.1 mol/L的氢硫酸溶液中存在平衡:
①H2S(aq) H+(aq)+HS-(aq);②HS-(aq)
H+(aq)+HS-(aq);②HS-(aq) H+(aq)+S2-(aq);
H+(aq)+S2-(aq);
(1)氢硫酸溶液中存在的离子有 。(不完整不给分)
(2)若向H2S溶液中( )
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO2气体,平衡向左移动,溶液pH增大
C.滴加新制氯水,平衡向左移动,溶液pH减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
Ⅱ.25℃时,部分物质的电离平衡常数如表所示:
化学式 | C | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH的电离平衡常数表达式 。
(2)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为 。
(3)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数 (填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是 。

Ⅲ.在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH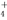 )=c(Cl-),则溶液显 性(填“酸”、“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb= 。
)=c(Cl-),则溶液显 性(填“酸”、“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb= 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:实验题
某实验小组欲用酸性KMnO4和H2C2O4反应通过测定单位时间内生成 CO2的量来探究影响反应速率的因素,设计实验方案如下:
实验序号 | A 溶液 | B 溶液 |
① | 20 mL 0.1 mol•L-1 H2C2O4 溶液 | 30 mL 0.01 mol•L-1 KMnO4 酸性溶液 |
② | 20 mL 0.2 mol•L-1 H2C2O4 溶液 | 30 mL 0.01 mol•L-1 KMnO4 酸性溶液 |

(1)检验上图装置气密性的最简便方法为:____________。
(2)H2C2O4溶液与酸性 KMnO4溶液反应的化学方程式为____________。
(3)该实验探究的是___________因素对化学反应速率的影响,相同时间内针筒中所得CO2的体积大小关系是___________(填实验序号)。
(4)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=________(若忽略溶液混合前后体积的变化)。
(5)小组同学发现反应速率总是如上右图所示,积极探究t1~t2时间内速率变快的主要原因,提出假设可能是:①__________、②_________、③K+对该反应有催化作用。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上期中化学卷(解析版) 题型:选择题
下列有关物质用途的描述不符合事实的是
A.氢氧化铝可用于治疗胃酸过多 B.过氧化钠可用作潜水艇供氧剂
C.铝制容器可以贮运浓硝酸 D.甲醛可用作食品防腐剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com