
| A. | 在常温常压下,11.2L Cl2含有的分子数为0.5NA | |
| B. | 1 L 0.5 mol•L-1硝酸钡溶液中所含NO3-数为0.5 NA | |
| C. | 2.4g Mg与足量的氮气完全反应失去的电子数为0.2NA | |
| D. | 在标准状况下,11.2L H2O含有的分子数为0.5NA |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、求出硝酸钡的物质的量n=CV,然后根据1mol硝酸钡中含2molNO3-来计算;
C、求出镁的物质的量,然后根据反应后镁变为+2价来分析;
D、标况下,水为液态.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氯气的物质的量小于0.5mol,则分子数小于0.5NA个,故A错误;
B、溶液中硝酸钡的物质的量n=CV=0.5mol/L×1L=0.5mol,而1mol硝酸钡中含2molNO3-,故0.5mol硝酸钡中含1molNO3-即NA个,故B错误;
C、2.4g镁的物质的量为0.1mol,而反应后镁变为+2价,故0.1mol镁失去0.2mol电子即0.2NA个,故C正确;
D、标况下,水为液态,不能根据气体摩尔体积来计算其物质的量,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{71}{161}$×100% | B. | $\frac{w}{w+36a}$×100% | ||
| C. | $\frac{7100w}{161(w+18a)}$% | D. | $\frac{71w}{161(w+36a)}$×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3胶体、白磷、石灰乳 | B. | 干冰、铁、氯化氢 | ||
| C. | 烧碱、液态氧、碘酒 | D. | 空气、氮气、明矾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
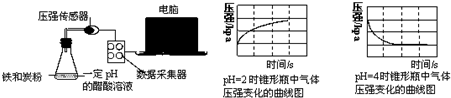
| A. | 析氢腐蚀和吸氧腐蚀的速率一样快 | |
| B. | 在酸性溶液中生铁可能发生吸氧腐蚀 | |
| C. | 溶液pH≤2时,生铁发生析氢腐蚀 | |
| D. | 两溶液中负极反应均为:Fe-2e-═Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分解反应一定是氧化还原反应 | |
| B. | 非金属单质在化学反应中一定是氧化剂 | |
| C. | 金属单质在化学反应中一定是还原剂 | |
| D. | 元素由化合态转化为游离态,该元素一定被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3和Na2O2 | B. | 只有Na2CO3 | C. | Na2CO3和NaOH | D. | Na2O和NaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com