
| A. | ClO-做还原剂 | B. | Fe(OH)3在反应中被还原 | ||
| C. | 高铁酸钾中铁的化合价为+7 | D. | 制备1molK2FeO4时转移3 mol 电子 |
分析 2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+5H2O中,Fe元素的化合价由+3价升高为+6价,Cl元素的化合价由+1价降低为-2价,以此来解答.
解答 解:A.Cl元素的化合价降低,则ClO-是氧化剂,故A错误;
B.Fe元素的化合价由+3价升高为+6价失去电子被氧化,则Fe(OH)3在反应中被氧化,故B错误;
C.高铁酸钾中铁的化合价为+6价,故C错误;
D.每生成1 mol高铁酸钾转移电子为1mol×(6-3)=3 mol,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子数的考查,题目难度不大.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2O含有的分子数为NA | |
| B. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA | |
| C. | 通常状况下,NA 个CO2分子占有的体积为22.4L | |
| D. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯银器表面在空气中因化学腐蚀渐渐变暗 | |
| B. | 当镀铜铁制品的镀层破损时,镀层仍能对铁制品起保护作用 | |
| C. | 铁制品长期与氯化铵溶液接触,易发生吸氧腐蚀 | |
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单体的结构简式为CH2═CHCOOR | B. | 在一定条件下能发生加成反应 | ||
| C. | 在一定条件下能发生水解反应 | D. | 没有固定熔沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在该反应中氧化剂与还原剂的物质的量之比为1:2 | |
| B. | 在该反应中,氧化产物有两种,还原产物有一种 | |
| C. | 若不考虑溶液体积变化,吸收尾气后,溶液的pH将增大 | |
| D. | 在该反应中,每消耗22.4LNO必转移2 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2H2(g)+O2(g)=2H2O(g);△H12H2(g)+O2(g)=2H2O(l);△H2 | |
| B. | S(g)+O2(g)=SO2(g);△H1S(s)+O2(g)=SO2(g);△H2 | |
| C. | CO(g)+$\frac{1}{2}$O2(g)=CO2(g);△H12CO(g)+O2(g)=2CO2(g);△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g);△H1$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g);△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
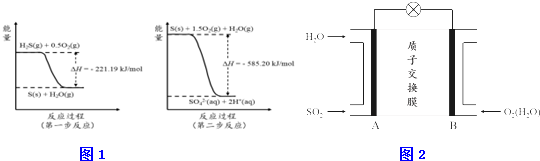
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NA个氮原子的氮气在标准状况下的体积约为11.2L | |
| B. | 25℃,1.01×105Pa,64g SO2中含有的原子数小于3NA | |
| C. | 在常温常压下,11.2LCl2含有的分子数为0.5NA | |
| D. | 标准状况下,11.2L H2O含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种溶液pH的大小顺序是①<②<③ | |
| B. | 若将3种溶液稀释相同倍数,pH变化最大的是③ | |
| C. | 若分别加入25mL0.1 mol•L-1盐酸后,pH最大的是② | |
| D. | 若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com