
橙花醇具有玫瑰及苹果香气,可作为香料,其结构简式如下
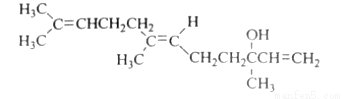
下列关于橙花醇的叙述,正确的是
A.橙花醇的分子式为C15H24O
B.在浓硫酸催化下加热脱水,可以生成不止一种四烯烃
C.在一定条件下能发生取代、催化氧化、酯化、加聚反应
D.0.1mo1橙花醇在室温下与溴的四氯化碳溶液反应,最多消耗0.3mo1Br2
 考前必练系列答案
考前必练系列答案科目:高中化学 来源:2015-2016学年河北省冀州市高一下期末文科化学A卷(解析版) 题型:选择题
根据元素在周期表中的位置判断,下列元素中原子半径最小的是( )
A. 氧 B. 氮 C. 碳 D. 氟
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三下热身考理综化学试卷(解析版) 题型:填空题
物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
(1)第二周期中,元素的第一电离能处于B与N之间的元素有_________种。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为_________________
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是_____________,1mol (C2H5O)3P=O分子中含有的σ键与π键的数目比为__________________。
(4)已知固态NH3、H2O、HF的氢键键能和结构如下:
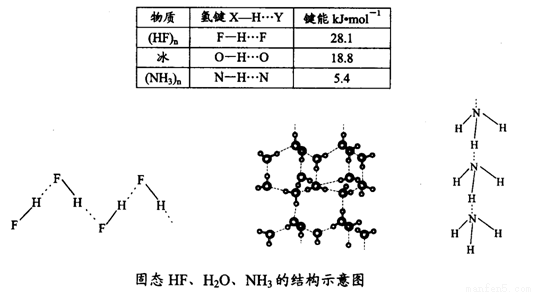
解释H2O、HF、NH3沸点依次降低的原因___________________。
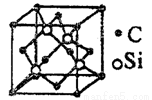
(5)碳化硅的结构与金刚石类似(如图所示),其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有___________个,与碳原子等距离最近的碳原子有__________个。已知碳化硅晶胞边长为a pm,则碳化硅的密度为__________g·cm3。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下第二次月考化学试卷(解析版) 题型:实验题
Ⅰ.莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。

(1)鞣酸的分子式是: ;莽草酸分子中有 个手性碳原子。
(2)写出莽草酸与Br2/CCl4溶液、鞣酸与足量氢氧化钠溶液反应的化学方程式:
;
。
Ⅱ.实验室也可用如图所示的装置制取少量乙酸乙酯。(已知乙酸乙酯在水中的溶解度较大,15℃时100g水中能溶解8.5g)

在100mL三颈瓶中,加入4mL乙醇,摇动下慢慢加入5mL浓硫酸,使其混合均匀,并加入几粒沸石。三颈瓶一侧口插入温度计,另一侧口插入恒压滴液漏斗,中间口安一长的刺形分馏柱(整个装置如右图)。
仪器装好后,在恒压滴液漏斗内加入10mL乙醇和8mL冰醋酸,混合均匀,先向瓶内滴入约2mL的混合液,然后,将三颈瓶在石棉网上小火加热到110~120℃左右,这时蒸馏管口应有液体流出,再从恒压滴液漏斗慢慢滴入其余的混合液,控制滴加速度和馏出速度大致相等,并维持反应温度在110~125℃之间,滴加完毕后,继续加热10分钟,直到温度升高到130℃不再有馏出液为止。试回答下列问题:
(3)使用恒压分液漏斗而不使用普通分液漏斗的原因是: 。
(4)在实验中控制三颈烧瓶中反应温度在120℃左右。理由是: 。
(5)滴加混合液时若速度过快,会使大量乙醇来不及反应而被蒸出,同时也造成 ,导致反应速度减慢。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下第二次月考化学试卷(解析版) 题型:选择题
某有机物A的化学式为C6H12O2,已知A~E有如图转化关系,且D不与Na2CO3溶液反应,C、E均能发生银镜反应,则A的结构可能有
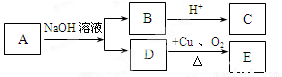
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源:2016届吉林省长春十一高三下考前冲刺理综化学试卷二(解析版) 题型:简答题
X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态.请回答下列问题:
(1)Q+核外电子排布式为___________;
(2)化合物X2W2中W的杂化方式为___________,ZW2-离子的立体构型是___________;
(3)Y、R的最高价氧化物的沸点较高的是___________(填化学式),原因是___________;
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为___________;
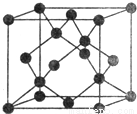
(5)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为___________,Y原子的配位数为___________,若晶胞的边长为a pm,晶体的密度为ρ g/cm3,则阿伏加德罗常数的数值为___________(用含a和ρ的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三毕业班最后一卷理综化学试卷(解析版) 题型:实验题
“侯氏制碱法”是我国化工行业历史长河中一颗璀璨明珠。
Ⅰ..纯碱的制备:用下图装置制取碳酸氢钠,再间接制得纯碱。
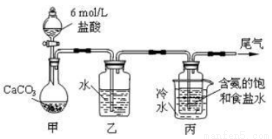
(1)装置乙的作用是 _________________,其中水可以用_______________代替;
(2)装置丙中反应的化学方程式为_____________________________________;
(3)用装置丙中产生的碳酸氢钠制取纯碱时,需要的实验操作有:_____________。
(4)定量分析:测定纯碱样品纯度
提供药品:酚酞、甲基橙、0.1mol/LHCl溶液
实验步骤:
①称取样品mg,溶于水形成100mL溶液;
②向溶液中滴加少量___________作指示剂,再向其中滴加盐酸溶液至终点,消耗盐酸_________VmL;
③计算:纯碱样品纯度=__________________。
Ⅱ.某小组同学在0.1mol/LNaHCO3溶液中滴加酚酞溶液1滴,溶液没有什么变化,但加热后显淡红色,加热较长时间后冷却,红色不褪去。为探究原因,进行了下列实验:加热0.1mol/LNaHCO3溶液,测得溶液pH随温度变化的曲线:
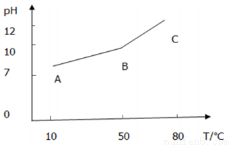
当温度恢复到10℃,测得溶液 pH=11.5。
(5)依据图像信息对下列问题做出合理猜测:
①AB段pH上升原因:____________________________________________________,
②BC段pH上升原因:____________________________________________________;
(6)设计实验对BC段pH上升的合理猜测进行验证(药品任意选择):__________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省宁波市高一下期中化学试卷(解析版) 题型:选择题
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是 ( )
A. 质子数c>b B. 离子的还原性Y2->Z-
C. 氢化物的稳定性H2Y>HZ D. 原子半径X<W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com