
| A. | 13g乙炔(C2H2)总原子数为2NA | |
| B. | 4℃时9mL水和11.2L氮气含有相同的分子数 | |
| C. | 同温同压下,NA个NO2与NA个N2的体积相等 | |
| D. | 标准状况下,11.2 L氧气所含的原子数目为NA |
分析 A.质量转化为物质的量结合1个乙炔分子含有2个碳原子解答;
B.4℃时水的密度为1g/mL,气体摩尔体积不等于22.4L/mol;
C.依据阿伏伽德罗定律内容分析,同温、同压、同物质的量的气体体积相同;
D.1个氧气分子含有2个氧原子.
解答 解:A.13g乙炔(C2H2)物质的量为$\frac{13g}{26g/mol}$=0.5mol,含有碳原子个数为0.5mol×2×NA=NA,故A错误;
B.4℃时9mL水质量为9g物质的量为0.5mol,11.2L氮气因Vm未知,无法计算物质的量,故B错误;
C.依据阿伏伽德罗定律内容分析,同温、同压、同物质的量的气体体积相同,NA个NO2与NA个N2和O2的混合气体的体积相等,故C正确;
D.标准状况下,11.2 L氧气物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,含有氧原子个数为NA,故D正确;
故选:CD.
点评 本题考查物质的量的有关计算,以及阿伏加德罗定律及推论,注意把握物质的量、质量、体积之间的计算公式的运用,注意气体摩尔体积使用条件和对象,题目难度不大.


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,原溶液一定有SO42- | |
| B. | 验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明有Cl- | |
| C. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,原溶液中一定有CO32- | |
| D. | 加入氯水后,滴加KSCN溶液,溶液变红,原溶液中一定有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | f.g.k.m | B. | c.j.k.m | C. | c.h.i.k | D. | f.g.h.j. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石>晶体硅>碳化硅 | B. | 氧化铝>氯化钾>氯化钠 | ||
| C. | CBr4>CCl4>CF4 | D. | AsH3>PH3>NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
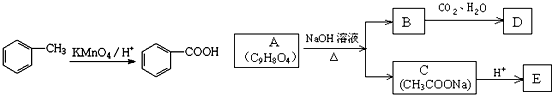
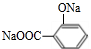 ,
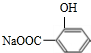
,

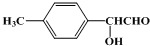 、
、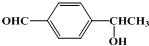
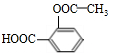 +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+2H2O.
+CH3COONa+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A分子的原子的核外电子排布式是1s22s22p63s23p4 | |
| B. | 向D的溶液中加入少量二氧化锰,一定有无色气体生成. | |
| C. | 还原性强弱B>C | |
| D. | 若将1mol E在氧气中完全燃烧,只生成1mol CO2和2molH2O,则E的分子式是CH4O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,Cl2的摩尔质量为71g | |
| B. | 氧化还原反应一定有氧元素参加 | |
| C. | 标准状况下,1 mol CCl4的体积是22.4L | |
| D. | Na2CO3属于钠盐,又属于碳酸盐是用交叉分类法分类的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com