
现有分别放置如图装置(都盛有稀H2SO4溶液)中的四个相同的纯锌片,腐蚀最慢的是()
A.  B.
B. 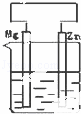 C.
C. 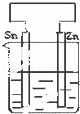 D.
D. 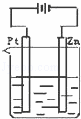
考点: 金属的电化学腐蚀与防护.
专题: 电化学专题.
分析: 电化学腐蚀较 化学腐蚀快,金属得到保护时,腐蚀较慢,作原电池正极和电解池阴极的金属被保护,腐蚀快慢为:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀.
化学腐蚀快,金属得到保护时,腐蚀较慢,作原电池正极和电解池阴极的金属被保护,腐蚀快慢为:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀.
解答: 解:A中发生化学腐蚀,B中锌作原电池正极,Zn被保护,C中锌作负极,发生电化学腐蚀,加快锌的腐蚀,D中锌作电解池阴极,不易被腐蚀,
腐蚀快慢为:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀,
则腐蚀速率由快到慢的顺序为CABD,
故选D.
点评: 本题考查不同条件下金属腐蚀的快慢,明确腐蚀快慢为:电解原理引起的腐蚀>原电池原理引 起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀即可解答,难度不大.
起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀即可解答,难度不大.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
已知A(g)+B(g)⇌C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ 700 800 830 1000 1200
平衡常数 1.7 1.1 1.0 0.6 0.4
回答下列问题:
(1)该反应的平衡常数表达式K=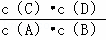 ,△H<0(填“<”“>”“=”);
,△H<0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol•L﹣1•s﹣1,则6s时c(A)=0.022 mol•L﹣1,C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 ,如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率为 ;
(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.压强不随时间改变
b.气体的密度不随时间变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等.
查看答案和解析>>
科目:高中化学 来源: 题型:
在c(H+):c(OH﹣)=1:2的水溶液中能大量共存的离子组是()
A. K+、Al3+、HCO3﹣、SO42﹣ B. Ca2+、NH4+、CO32﹣、Cl﹣
C. Na+、K+、NO3﹣、ClO﹣ D. Na+、Fe2+、I﹣、SO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关原子结构和元素周期律的表述正确的是()
①原子序数为15的元素的最高化合价为+3
②第ⅦA族元素是同周期中非金属性最强的元素
③第ⅥA族元素的原子最高正价等于主族序数
④原子序数为12的元素位于元素周期表的第三周期第ⅡA族.
A. ①② B. ①③ C. ②④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象预测正确的是()
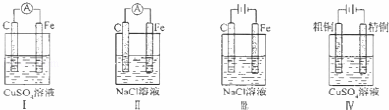
A. 实验Ⅰ:电流表A指针偏转,碳棒上有气泡冒出
B. 实验Ⅱ:电流表A指针偏转,铁极上有无色气体产生
C. 实验Ⅲ:碳棒上有无色气体产生,铁极上有黄绿色气体产生
D. 实验IV:粗铜溶解,精铜上有红色固体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:
(1)通甲烷的铂丝为原电池的极,发生的电极反应为 .
(2)该电池工作时(放电)反应的总化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
向10mL 0.1mol•L﹣1 NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是()
A. x=10时,溶液中有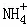 、Al3+、
、Al3+、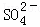 ,且c(
,且c(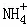 )=c(Al3+)
)=c(Al3+)
B. x=20时,溶液中所发生的反应离子方程式为:Al3++2SO42﹣+2Ba2++4OH﹣═2BaSO4↓+AlO2﹣+2H2O
C. x=30时,溶液中有Ba2+、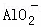 、OH﹣,且c(OH﹣)>c(
、OH﹣,且c(OH﹣)>c(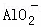 )
)
D. 滴加过程中,生成沉淀的最大物质的量为0.003mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应速率的说法正确的是()
A. 化学反应速率是指一定时间内任何一种反应物浓度的减少或者任何一种生成物浓度的增加
B. 化学反应速率为“0.8mol/(L•s)”表示的意思是:时间为1s时,某物质的浓度为0.8mol/L
C. 根据化学反应速率的大小可以知道化学反应进行的快慢
D. 对于任何化学反应来说,反应速率越大,反应现象越明显
查看答案和解析>>
科目:高中化学 来源: 题型:
为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验.下列叙述中不正确的是()
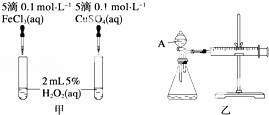
A. 图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小
B. 若图甲所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C. 用图乙所示装置测定反应速率,可测定反应产生的气体体积及反应时间
D. 为检查图乙所示装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com