
【题目】在15g铁和氧化铁的混合物中加入150mL稀H2SO4放出氢气1.68L(标准状况)。当反应停止后,铁和氧化铁均无剩余,且溶液中无Fe3+存在。为了中和过量H2SO4,并使Fe2+完全转化为Fe(OH)2沉淀,共耗用3 mol/L NaOH溶液200mL。求:
(1)混合物中铁的质量为 g
(2)稀H2SO4的物质的量浓度为 mol·L-1
【答案】(1)7(2) 2
【解析】
试题分析:(1)铁和氧化铁与硫酸反应均无剩余,且溶液中无Fe3+存在,反应生成FeSO4,生成氢气为![]() =0.075mol,
=0.075mol,
设Fe、氧化铁的物质的量分别为xmol、ymol,则:
根据二者质量,可得:56x+160y=15
根据电子转移守恒,可得:2x=2y+0.075×2
联立方程,解得x=0.125,y=0.05
故m(Fe)=0.125mol×56g/mol=7g;
(2)铁和氧化铁与硫酸反应后溶液中溶质为FeSO4、H2SO4,加入NaOH使Fe2+完全转化为Fe(OH)2沉淀,产生反应后的溶液溶质只有Na2SO4,根据硫酸根守恒则n(H2SO4)=n(Na2SO4),根据钠离子守恒则n(Na2SO4)=![]() n(NaOH)=
n(NaOH)=![]() ×3mol/L×0.2L=0.3mol,c(H2SO4)=
×3mol/L×0.2L=0.3mol,c(H2SO4)=![]() =2mol/L。
=2mol/L。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的可再生能源。
(1)已知2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH =a kJ·mol-1
CO(g)+2H2(g)=CH3OH(g) ΔH =b kJ·mol-1
试写出由CH4和O2制取甲醇的热化学方程式 。
(2)还可通过下列反应制甲醇:CO(g)+2H2(g)![]() CH3OH(g)。甲图是反应时CO和CH3OH(g)的浓度随时间的变化情况。从反应开始到达平衡,用H2表示反应速率υ(H2)= 。
CH3OH(g)。甲图是反应时CO和CH3OH(g)的浓度随时间的变化情况。从反应开始到达平衡,用H2表示反应速率υ(H2)= 。
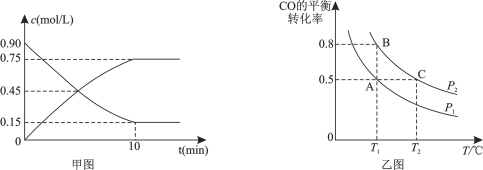
(3)在一容积可变的密闭容器中充入10 mol CO和20 mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如乙图所示。
①下列说法能判断该反应达到化学平衡状态的是_______(填字母)。
A.H2的消耗速率等于CH3OH的生成速率的2倍
B.H2的体积分数不再改变
C.体系中H2的转化率和CO的转化率相等
D.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA________PB(填“>、<、=”)。
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10 molCO和20 molH2,则在平衡状态B时容器的体积V(B)= L。
(4)以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)。
①若KOH溶液足量,则写出电池负极反应式________________________。
②若电解质溶液中KOH的物质的量为0.8 mol,当有0.5 mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、G是元素周期表中原子序数依次增大的五种元素。X元素是元素周期表中核电荷数最小的元素。Y的一种核素常用于考古,其一种同素异形体为自然界最硬的物质。ZX3气体溶于水呈碱性。W的外围电子排布是3s1。G2+离子的M层d轨道只有5个电子。请回答下列问题:
(1)W在元素周期表中的位置是 ;W和Z形成的化合物水溶液呈碱性,用离子方程式表示其原因 。
(2)Z原子的第一电离能比氧原子的 (填“大”或“小”);G的基态原子电子排布式是
(3)X与Y可形成多种化合物,其中一种化合物的分子式是X6Y6,分子中只有σ键,该分子的结构简式是 ;该化合物中Y的杂化轨道类型是 。
(4)G的最高价氧化物对应水化物的钾盐,在酸性条件下,常用于测定溶液中Fe2+的含量,该反应的离子方程式是
(5)可用YX4还原ZOx以消除其污染。已知:
YX4(g) +4ZO2(g)=4ZO(g)+YO2(g)+2X2O(g) △H=" -" 574 kJ·mol-1
YX4(g)+4ZO(g)=2Z2(g)十YO2(g) +2X2O(g) △H =" -1160" kJ·mol-1
试写出用YX4还原ZO2至Z2的热化学方程式___ _。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiCl4是生产金属钛和钛白的原料,工业上主要用TiO2氯化的方法来制取。某化学实验小组以8.0g TiO2和足量 CCl4为原料制取TiCl4。装置图如下:
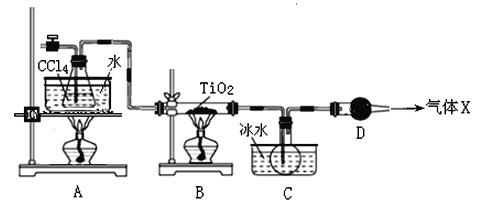
下表是有关物质的性质:
物质 | 熔点/℃ | 沸点/℃ | 其他 |
CCl4 | ﹣23 | 76.8 | 与TiCl4互溶 |
TiCl4 | ﹣25 | 136 | 遇潮湿空气产生白雾 |
请回答下列问题
(1)TiCl4中化学键的类型是 。
(2)B中TiO2发生反应的化学方程式是 。
(3)X气体的主要成分是 。
(4)实验开始时先点燃A处的酒精灯,待C中烧瓶里有液滴出现时再点燃B处的酒精灯,其主要目的是 。
(5)欲分离C装置中的TiCl4,应采用的实验操作为 (填操作名称)。
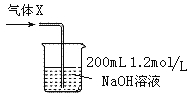
(6)若将反应过程中生成的气体X全部通入到下图所示的装置中充分反应,生成的盐是 (填化学式),生成盐的总物质的量n≤ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学一选修5:有机化学基础]铃兰醛具有甜润的百合香味,对皮肤的刺激性小,对碱稳定,广泛用于百合、丁香、玉兰、茶花以及素心兰、东方型香型日用香精的合成。常用作肥皂、洗涤剂的香料,还可用作花香型化妆品的香料。其合成路线如下图所示:

(1)B中官能团的名称是 ;
(2)④的反应类型是 ;
(3)写出反应②的化学方程式 ;
(4)乌洛托品的结构式如图所示,其二氯取代物有 种;

将甲醛的水溶液与氨水混合蒸发可制得乌洛托品,该反应的化学方程式 ;
(5)写出满足下列条件的A的同分异构体
Ⅰ.有两个取代基; Ⅱ.取代基在邻位。
(6)已知:![]() 。仿照上述流程,写出以CH3CH2CHO为原料制备聚乳酸
。仿照上述流程,写出以CH3CH2CHO为原料制备聚乳酸 的合成路线流程图(无机试剂可以任选):
的合成路线流程图(无机试剂可以任选):
CH3CH2CHO→ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。
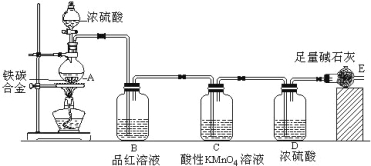
(1)m g铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:
①常温下碳与浓硫酸不反应;② 。
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式 。
(3)C装置的作用 。
(4)该小组同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能会导致铁质量分数测量值偏低的是 。
A.A中反应不完全
B.E中碱石灰会吸收空气中的CO2和H2O
C.反应生成的SO2部分被E中碱石灰吸收
D.反应完全后,还有CO2气体滞留在装置体系中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,总反应为:2CH3CHO + H2O![]() CH3CH2OH + CH3COOH
CH3CH2OH + CH3COOH
实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如右图所示。
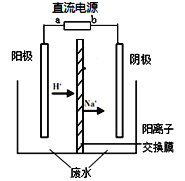
(1)若以甲烷燃料电池为直流电源,则燃料电池中b极应通入 (填化学式)气体。
(2)电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体。电极反应如下:
阳极:① 4OH--4e-=O2↑+2H2O
② 。
阴极:① 。
②CH3CHO+2e-+2H2O=CH3CH2OH+2OH-
(3)电解过程中,阴极区Na2SO4的物质的量 (填“增大”、“减小”或“不变”)。
(4)电解过程中,某时刻测定了阳极区溶液中各组分的物质的量,其中Na2SO4与CH3COOH的物质的量相同。下列关于阳极区溶液中各微粒浓度关系的说法正确的是 (填字母序号)。
a. c(Na+)不一定是c(SO42-)的2倍
b. c(Na+)=2c(CH3COOH)+2c(CH3COO-)
c. c(Na+)+c(H+)=c(SO42-)+c(CH3COO-)+c(OH-)
d. c(Na+)>c(CH3COOH)>c(CH3COO-)>c(OH-)
(5)已知:乙醛、乙醇的沸点分别为20.8℃、78.4℃。从电解后阴极区的溶液中分离出乙醇粗品的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向可变容积的密闭容器中通入N2和H2,发生反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0达到平衡后,容器的体积为4L,试回答下列问题:
2NH3(g) △H<0达到平衡后,容器的体积为4L,试回答下列问题:
(1)该条件下,反应的平衡常数表达式K = ,若降低温度,K值将 (填“增大”、“减小”或“不变”)。
(2)达到平衡后,若其它条件不变,把容器体积缩小一半,平衡将___(填“向逆反应方向”、“向正反应方向”或“不”)移动,平衡常数K将 (填“增大”“减小”或“不变”),理由是___________________________。
(3) 达到平衡后,在恒压条件下,向容器中通入氦气(He),氮气的转化率将________(填“增大”、“减小”或“不变”)。
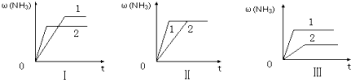
(4)在三个相同的容器中各充入1 molN2和3molH2,在不同条件下分别达到平衡,氨的体积分数ω随时间变化如图。下列说法正确的是 (填序号)。
a.图Ⅰ可能是不同压强对反应的影响,且P2>P1
b.图Ⅱ可能是同温同压下催化剂对反应的影响,且催化性能1>2
c.图Ⅲ可能是不同温度对反应的影响,且T1>T2
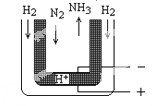
(5)常压下,把H2和用He稀释的N2分别通入一个570℃的电解池装置(下图),H2和N2便可在电极上合成氨,装置中的电解质(图中黑细点处)能传导H+,则阴极的电极反应式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5:有机化学基础】
阿立呱陛(A)是一种新的抗精神分裂症药物,可由化合物B, C, D在有机溶剂中通过
以下两条路线合成得到。

(1)E的结构简式为 ,其含氧官能团有 (写名称)o
(2)由C, D生成化合物F的反应类型是 。化合物C与足量的NaOH乙醇溶液共热反应的产物的名称是
(3)H属于氨基酸,与B的水解产物互为同分异构体。H能与FeCl3溶液发生显色反应,且苯环上的一氯代物只有2种。写出两种满足上述条件的H的结构简式: 、
(4)合成F(相对分子质量为366)时还可能生成一种相对分子质量为285的副产物G,G能使漠水褪色,G的结构简式为
(5)已知: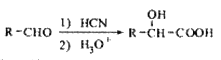 写出由C制备化合物
写出由C制备化合物 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com