
| A. | +283.5 kJ•mol-1 | B. | -172.5 kJ•mol-1 | C. | +172.5 kJ•mol-1 | D. | -504 kJ•mol-1 |
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 | B. | 1.0 mol•L-1 | C. | 0.3 mol•L-1 | D. | 0.4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 中和热是在稀溶液中,酸和碱反应生成1mol水所放出的热量.某同学利用50mL 0,.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和热测定的实验,回答下列问题:
中和热是在稀溶液中,酸和碱反应生成1mol水所放出的热量.某同学利用50mL 0,.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和热测定的实验,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
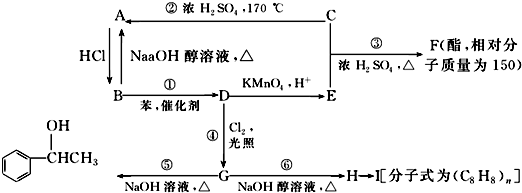
 .
. ;
; .
.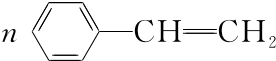 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$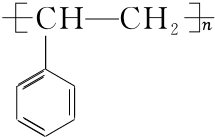 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④① | B. | ④②③① | C. | ④③①② | D. | ②①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ④⑥ | C. | ①④⑥ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
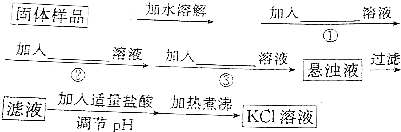
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com