
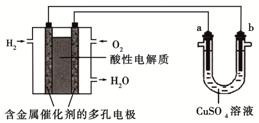
| A. | 燃料电池工作时,正极反应为:O2+2H2O+4e-═4OH- | |
| B. | a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 | |
| C. | a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 | |
| D. | a、b两极均是石墨时,a极上产生的O2与电池中消耗的H2的体积比为2:1 |
分析 左边装置是氢氧燃料电池,所以是原电池,原电池放电时,燃料失电子发生氧化反应,所以投放燃料的电极为负极,投放氧化剂的电极为正极,正极上氧化剂得电子发生还原反应,由于电解质溶液呈酸性,正极反应为:O2+4e-+4H+=2H2O;右边装置有外接电源,所以是电解池,连接负极的b电极是阴极,连接正极的a电极是阳极,阳极上失电子发生氧化反应,阴极上得电子发生还原反应.
解答 解:A.由于电解质溶液呈酸性,正极发生还原反应,氧气被还原生成水,电极反应为:O2+4e-+4H+=2H2O,故A错误;
B.a极是铁,b极是铜时,铁被氧化,b极上有铜析出,故B错误;
C.若a极是粗铜,b极是纯铜时,a极上比Cu活泼的金属先失去电子,a极逐渐溶解,b极上只析出Cu,故C正确;
D.a、b两极均是石墨时,在相同条件下,电子转移量相等,a极产生的气体为氧气,产生1molO2需4mol电子,所以需要燃料电池的2molH2,a极上产生的O2与电池中消耗的H2的体积比为1:2,故D错误.
故选C.
点评 本题考查原电池和电解池知识,为高考常见题型和高频考点,侧重于学生的分析能力和计算能力的考查,易错点为A,注意电解质的酸碱性,为解答该题的关键.题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 4 | B. | 6 | C. | 8 | D. | 12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag是还原剂 | B. | O2被还原 | C. | H2S发生氧化反应 | D. | Ag2S是氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
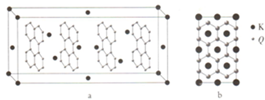
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
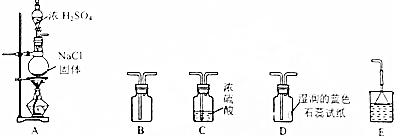
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用大理石和稀盐酸反应制CO2:CO32-+2H+═CO2↑+H2O | |
| B. | Cl2通入石灰乳中:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 氢氧化钠溶液腐蚀玻璃:2OH-+SiO2═SiO32-+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com