
(10分)(1)CCS技术是将工业和有关能源产业中所生产的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天燃气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
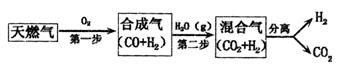
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1gCH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式 。
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用(1)转化中得到的合成气制备甲醇。反应为CO(g)+2H2(g)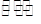 CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:
CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:
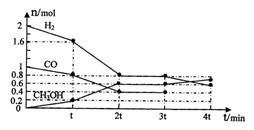
①根据上图计算,从反应开始到tmin时,用H2浓度变化表示的平均反应速率v(H2)=
②t min至2tmin时速率变化的原因可能是 ;
③3tmin时对反应体系采取了一个措施,至4tmin时CO的物质的量为0.5mol,请完成上图CO的曲线。
(3)某同学按下图所示的装置用甲醇燃料电池(装置Ⅰ)进行电解的相关操作,以测定铜的相对原子质量,其中c电极为铜棒,d电极为石墨,X溶液为500mL0.4mol/L硫酸铜溶液。当装置Ⅱ中某电极上收集到标准状况下的气体V1mL时,另一电极增重mg(m<12.8)。
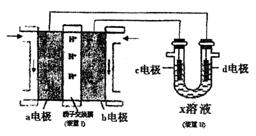
①装置Ⅰ中、H+向 极(填“a”或“b”)移动;b电极上发生的反应为 。
②铜的相对原子质量的表达式为 (用m和V1的代数式表示)。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
(10分)(1)CCS技术是将工业和有关能源产业中所生产的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天燃气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1gCH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式 。
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用(1)转化中得到的合成气制备甲醇。反应为CO(g)+2H2(g)![]() CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:
CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:
①根据上图计算,从反应开始到tmin时,用H2浓度变化表示的平均反应速率v(H2)=
②t min至2tmin时速率变化的原因可能是 ;
③3tmin时对反应体系采取了一个措施,至4tmin时CO的物质的量为0.5mol,请完成上图CO的曲线。
(3)某同学按下图所示的装置用甲醇燃料电池(装置Ⅰ)进行电解的相关操作,以测定铜的相对原子质量,其中c电极为铜棒,d电极为石墨,X溶液为500mL0.4mol/L硫酸铜溶液。当装置Ⅱ中某电极上收集到标准状况下的气体V1mL时,另一电极增重mg(m<12.8)。
①装置Ⅰ中、H+向 极(填“a”或“b”)移动;b电极上发生的反应为 。
②铜的相对原子质量的表达式为 (用m和V1的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)(1)CCS技术是将工业和有关能源产业中所生产的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天燃气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1gCH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式 。
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用(1)转化中得到的合成气制备甲醇。反应为CO(g)+2H2(g)![]() CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:
CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:
①根据上图计算,从反应开始到tmin时,用H2浓度变化表示的平均反应速率v(H2)=
②t min至2tmin时速率变化的原因可能是 ;
③3tmin时对反应体系采取了一个措施,至4tmin时CO的物质的量为0.5mol,请完成上图CO的曲线。
(3)某同学按下图所示的装置用甲醇燃料电池(装置Ⅰ)进行电解的相关操作,以测定铜的相对原子质量,其中c电极为铜棒,d电极为石墨,X溶液为500mL0.4mol/L硫酸铜溶液。当装置Ⅱ中某电极上收集到标准状况下的气体V1mL时,另一电极增重mg(m<12.8)。
①装置Ⅰ中、H+向 极(填“a”或“b”)移动;b电极上发生的反应为 。
②铜的相对原子质量的表达式为 (用m和V1的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2012届山东省莱州一中高三第三次质量检测化学试卷 题型:填空题
(10分)(1)CCS技术是将工业和有关能源产业中所生产的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天燃气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物 质未标出)。回答下列问题:
质未标出)。回答下列问题: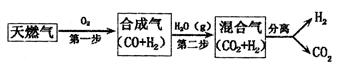
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1gCH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式 。
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用(1)转化中得到的合成气制备甲醇。反应为CO(g)+2H2(g)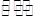 CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:
CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图: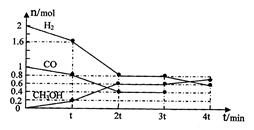
①根据上图计算,从反应开始到tmin时,用H2浓度变化表示的平均反应速率v(H2)=
②t min至2tmin时速率变化的原因可能是 ;
③3tmin时对反应体系采取了一个措施,至4tmin时CO的物质的量为0.5mol,请完成上图CO的曲线。
(3)某同学按下图所示的装置用甲醇燃料电池(装置Ⅰ)进行电解的相关操作,以测定铜的相对原子质量,其中c电极为铜棒,d电极为石墨,X溶液为500mL0.4mol/L硫酸铜溶液。当装置Ⅱ中某电极上收集到标准状况下的气体V1mL时,另一电极增重mg(m<12.8)。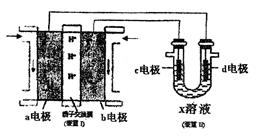
①装置Ⅰ中、H+向  极(填“a”或“b”)移动;b电极上发生的反应为 。
极(填“a”或“b”)移动;b电极上发生的反应为 。
②铜的相对原子质量的表 达式为 (用m和V1的代数式表示)。
达式为 (用m和V1的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省高三第三次质量检测化学试卷 题型:填空题
(10分)(1)CCS技术是将工业和有关能源产业中所生产的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天燃气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:

CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1gCH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式 。
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用(1)转化中得到的合成气制备甲醇。反应为CO(g)+2H2(g) CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:
CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:
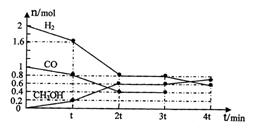
①根据上图计算,从反应开始到tmin时,用H2浓度变化表示的平均反应速率v(H2)=
②t min至2tmin时速率变化的原因可能是 ;
③3tmin时对反应体系采取了一个措施,至4tmin时CO的物质的量为0.5mol,请完成上图CO的曲线。
(3)某同学按下图所示的装置用甲醇燃料电池(装置Ⅰ)进行电解的相关操作,以测定铜的相对原子质量,其中c电极为铜棒,d电极为石墨,X溶液为500mL0.4mol/L硫酸铜溶液。当装置Ⅱ中某电极上收集到标准状况下的气体V1mL时,另一电极增重mg(m<12.8)。
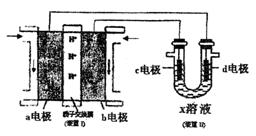
①装置Ⅰ中、H+向 极(填“a”或“b”)移动;b电极上发生的反应为 。
②铜的相对原子质量的表达式为 (用m和V1的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com