
| A. | 乙酸异丙酯 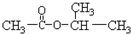 | B. | 乙酸叔丁酯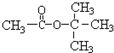 | C. | 对二甲苯 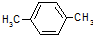 | D. | 均三甲苯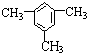 |
分析 在核磁共振氢谱中能出现两组峰,说明该分子中含有两类氢原子,且其峰面积之比为3:1,说明这两类氢原子的个数比是3:1,据此分析解答.
解答 解:A.乙酸异丙酯的结构简式为: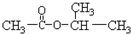 ,该分子的核磁共振氢谱中有三组峰,其峰面积之比是6:3:1,故A错误;
,该分子的核磁共振氢谱中有三组峰,其峰面积之比是6:3:1,故A错误;
B.乙酸叔丁酯的结构简式为: ,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:1,故B正确;
,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:1,故B正确;
C.对二甲苯的结构简式为: ,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:2,故C错误;
,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:2,故C错误;
D.均三甲苯的结构简式为: ,该分子的核磁共振氢谱中有两组峰,其面积之比是3:1,故D正确;
,该分子的核磁共振氢谱中有两组峰,其面积之比是3:1,故D正确;
故选BD.
点评 本题考查有机物的结构,明确核磁共振氢谱中吸收峰的组数、面积之比的含义是解本题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 尽量不使用一次性竹、木筷子 | |
| B. | 多挖煤,多发电,加快经济发展 | |
| C. | 利用特殊材料建屋顶、墙面,充分利用太阳光照明 | |
| D. | 提倡骑自行车、乘公交车出行 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将氨通入盐酸中:NH3+H+=NH4+ | |
| B. | 在稀NaOH溶液中滴入几滴NH4Cl溶液:NH4++OH-=NH3↑+H2O | |
| C. | 将少量铜屑放入浓硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O | |
| D. | 将稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X2+2Y2 ?2XY2 | B. | 2X2+Y2 ?2X2Y | C. | 3X2+Y2?2X3Y | D. | X2+3Y2?2XY3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
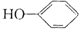 合成
合成 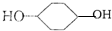
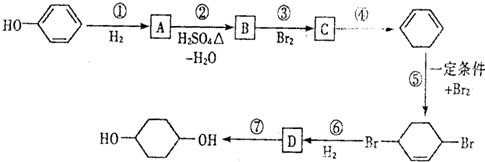
 ,D
,D .
.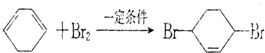 写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学反应方程式
写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学反应方程式 .
.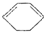 的反应方程式(有机物写结构简式,注明反应条件).
的反应方程式(有机物写结构简式,注明反应条件). .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
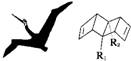 始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞翔的鸟,其键线式如图,其中R1、R2为烷烃基.则下列有关始祖鸟烯的说法中正确的是( )
始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞翔的鸟,其键线式如图,其中R1、R2为烷烃基.则下列有关始祖鸟烯的说法中正确的是( )| A. | 始祖鸟烯与CH2═CH-CH═CH2互为同系物 | |
| B. | 若R1、R2为-CH3,则其化学式为C12H16 | |
| C. | 若R1═R2,一定条件下烯烃双键碳原子上的氢也能取代,则始祖鸟烯环上的二氯代物有10种 | |
| D. | 始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,其褪色原理是一样的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①② | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
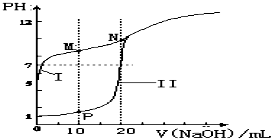 在弱电解质溶液中存在电离平衡,试回答下列问题.
在弱电解质溶液中存在电离平衡,试回答下列问题.| n(SO32-):n(HSO3-) | 91:1 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com