
【题目】磷能形成多种含氧酸。
(1)一元中强酸次磷酸(H3PO2)是一种精细化工产品,向10 mL H3PO2溶液中加入10 mL等物质的量浓度的NaOH溶液后,所得的溶液中只有H2PO2-、OH-两种阴离子。
① 写出H3PO2溶液与足量NaOH 溶液反应后形成的正盐的化学式:_______,该正盐溶液中各离子浓度由大到小的顺序为____________。
② 若25℃时,K (H3PO2) = 1×10-2,则0.01 mol · L-1的H3PO2溶液的pH =________。
(2)亚磷酸(H3PO3)是二元中强酸,25℃时亚磷酸的电离常数为K1= 3.7×10-2、K2=2.6×10-7。
试从电离平衡移动的角度解释K1、K2数据的差异______________。
(3) 25 ℃时,HF的电离常数为K = 3.6×10-4; H3PO4的电离常数为K1=7.5×10-3,K2=6.2×10-8,K3=4.4×10-13。足量NaF溶液和H3PO4溶液反应的离子方程式为______。
(4)相同温度下,等物质的量浓度的上述三种磷的含氧酸中。c(H+)由大到小的顺序为______________________________________________________(用酸的分子式表示)。
【答案】NaH2PO2 c(Na+)>c(H2PO2-)>c(OH-)>c(H+) 2 H3PO3第一步电离出的H+对第二步电离起到抑制作用 F- +H3PO4 =HF+H2PO4- H3PO3 >H3PO2 >H3PO4
【解析】
(1)①向10mL H3PO2溶液中加入10mL等物质的量浓度的NaOH溶液后,所得的溶液中只有H2PO2-、OH-两种阴离子,H3PO2是一元中强酸,H3PO2溶液与足量NaOH 溶液反应后形成的正盐为NaH2PO2;
酸根离子水解导致溶液呈碱性,但其水解程度较小;
②该溶液中c(H+)=![]() ,pH=-lgc(H+);
,pH=-lgc(H+);
(2)第一步电离出的氢离子抑制第二步电离;
(3)HF的电离平衡常数小于磷酸的第一步电离平衡常数大于其第二步、第三步电离平衡常数,所以NaF和磷酸反应生成HF和磷酸二氢钠;
(4)相同浓度的这三种含磷的酸中,其电离平衡常数越大,氢离子浓度越大。
(1)①向10mL H3PO2溶液中加入10mL等物质的量浓度的NaOH溶液后,所得的溶液中只有H2PO2-、OH-两种阴离子,H3PO2是一元中强酸,H3PO2溶液与足量NaOH 溶液反应后形成的正盐为NaH2PO2;
酸根离子水解导致溶液呈碱性,但其水解程度较小,离子浓度大小顺序是c(Na+)>c(H2PO2-)>c(OH-)>c(H+);
②该溶液中c(H+)=![]() ,pH=-lgc(H+)=-lg
,pH=-lgc(H+)=-lg![]() =2;
=2;
(2)第一步电离出的氢离子抑制第二步电离,所以第一步电离平衡常数与第二步电离平衡常数相差较大,因为:H3PO3第一步电离出的H+对第二步电离起到抑制作用;
(3)HF的电离平衡常数小于磷酸的第一步电离平衡常数大于其第二步、第三步电离平衡常数,所以NaF和磷酸反应生成HF和磷酸二氢钠,离子方程式为F-+H3PO4=HF+H2PO4-;
(4)相同浓度的这三种含磷的酸中,其电离平衡常数越大,氢离子浓度越大,电离平衡常数(多元酸看第一步电离平衡常数)H3PO3>H3PO2>H3PO4,则酸性H3PO3>H3PO2>H3PO4,相同浓度的这几种酸中氢离子浓度H3PO3>H3PO2>H3PO4。


科目:高中化学 来源: 题型:
【题目】下列反应在任何温度下均能自发进行的是
A. 2N2(g)+O2(g)===2N2O(g) ΔH=+163 kJ·mol-1
B. Ag(s)+Cl2(g)===AgCl(s) ΔH=-127 kJ·mol-1
C. HgO(s)===Hg(l)+O2(g) ΔH=+91 kJ·mol-1
D. H2O2(l)===O2(g)+H2O(l) ΔH=-98 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学通过如下流程制备氧化亚铜:

已知CuCl难溶于水和稀硫酸:Cu2O+2H+==Cu2++Cu+H2O
下列说法不正确的是
A. 步骤②SO2可用Na2SO3替换
B. 步骤③中为防止CuCl被氧化,可用SO2水溶液洗涤
C. 步骤④发生反应的离子方程式为2CuCl+2OH-=Cu2O+2Cl-+H2O
D. 如果Cu2O试样中混有CuCl和CuO杂质,用足量稀硫酸与Cu2O试样充分反应,根据反应前、后固体质量可计算试样纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是

A. 电子从b流出,经外电路流向a
B. HS-在硫氧化菌作用下转化为SO42-的反应是HS-+4H2O-8e-=SO42-+9H+
C. 如果将反应物直接燃烧,能量的利用率不会变化
D. 若该电池电路中有0.4mol电子发生转移,则有0.5molH+通过质子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷和镍均为重要的无机材料,在化工领域具有广泛的应用。
(1)基态As原子的价层电子的电子云轮廓图形状为_____________。与砷同周期的主族元素的基态原子中,第一电离能最大的为_____________(填元素符号。)
(2)Na3AsO3可用于碘的微量分析。
①Na+的焰色反应呈黄色,金属元素能产生焰色反应的微观原因为__________________________。
②Na3AsO3中所含阴离子的立体构型为_____________,写出一种与其互为等电子体的分子:_____________(填化学式)。
(3) 可用于合成Ni2+的配体,M中C原子的杂化方式为___________,其所含
可用于合成Ni2+的配体,M中C原子的杂化方式为___________,其所含![]() 键和π键的数目之比为___________。
键和π键的数目之比为___________。
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为___________。区分晶体Ni和非晶体Ni的最可靠的科学方法为___________。
(5)某砷镍合金的晶胞结构如下图所示,设阿伏加德罗常数的值为NA,则该晶体的密度ρ=___________g·cm-3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将20mL 0.10 mol/LCH3COOH溶液和20mL 0.10 mol/LHX溶液分别与20mL 0.10 mol/LNaHCO3溶液混合,测得产生气体的体积(V)随时间(t)变化如下图,下列说法中不正确的是
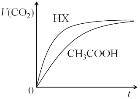
A. 反应开始前,HX溶液中c(H+)大于CH3COOH中c(H+)
B. CH3COOH溶液反应结束后,c(Na+)>c(CH3COO—)
C. 反应结束后所得两溶液中,c(CH3COO—)<c(X—)
D. 由该实验可知HX为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定容积的密闭容器中,可逆反应: mA(气)+nB(气) ![]() pC(气)+qD(气),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化, ②体系的密度不再发生变化, ③各组分的物质的量浓度不再改变, ④各组分的质量分数不再改变,⑤反应速率vA:vB:vC:vD=m:n:p:q,其中,能说明反应已达到平衡的是
pC(气)+qD(气),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化, ②体系的密度不再发生变化, ③各组分的物质的量浓度不再改变, ④各组分的质量分数不再改变,⑤反应速率vA:vB:vC:vD=m:n:p:q,其中,能说明反应已达到平衡的是
A. ③④ B. ②③④ C. ①②③④ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能被视为最具发歸力的清洁能源,开发新型储氣材料是氢能利用的重要研究方向。请回答下列问题:
Ⅰ.化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如 下反应制得:3CH4+2 (HB=NH) 3+6H2O=3CO2+6H3BNH3
(1)基态B原子的价电子排布式为___________,B、C, N, O第一电离能由大到小的顺序为_________,CH4、H2O、CO2的键角按照由大到小的顺序排列为___________。
(2)与(HB=NH)3,互为等电子体的有机分子为___________(填分子式)。
Ⅱ.氢气的安全贮存和运输是氢能应用的关键。
(1)印度尼赫鲁先进科学研宄中心的Datta和Pati等人借助ADF软件对一种新 型环烯类储氢材料(C16S8)进行研宄,从理论角度证明这种材料的分子呈平面结构(如图),每个杂环平面上下两侧最多可吸附10个H2分子。

①C16S8分子中C原子和S原子的杂化轨道类型分别为___________。
②相关键长数据如表所示:
化学键 | C-S | C=S | C16S8中碳硫键 |
键长/pm | 181 | 155 | 176 |
从表中数据看出,C16S8中碳硫键键长介于C—S键与C=S键之间,原因可能______________________。
③C16S8与H2微粒间的作用力是___________。
(2)有储氢功能的铜合金晶体具有立方最密堆积结构,晶胞中Cu原子位于面心,Ag 原子位于顶点,氢原子可进到由Cu原子与Ag原子构成的四面体空隙中。该晶体储氢后的晶胞结构与CaF2(如图)相似,该晶体储氢后的化学式为___________。


(3)MgH2是金属氢化物储氢材料,其晶胞如上图所示,该晶体的密度为agcm-3,则晶胞的体积为___________cm3(用含a、NA的代数式表示,NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 已知冰的熔化热为6.0kJ·mol-1,冰中氢键键能为20kJmol-1,假设每摩尔冰中有2mol氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键
B. 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为a,Ka=(ca)2/c(1-a)。若加水稀释,,则CH3COOH![]() CH3COO-+H+向右移动,a增大,Ka不变
CH3COO-+H+向右移动,a增大,Ka不变
C. 甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1
D. 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com