
下列实验操作或实验所得出的结论正确的是()
A. 
实验室中浓硝酸应保存在棕色细口瓶中,并贴有如图所示标签
B. 制备Fe(OH)3胶体时,应向沸水中逐滴加入1mol•L﹣1的FeCl3溶液,并继续加热到液体呈透明的红褐色为止
C. 用托盘天平称取5.85g NaCl,称量时砝码放在右盘,氯化钠放在左盘
D. 用50mL量筒量取5.6mL浓硫酸
E. 用四氯化碳萃取碘水中的碘,分液时有机层从分液漏斗的下端放出
F. 用广泛pH试纸测得某溶液的pH为4.8
考点: 化学试剂的分类;胶体的重要性质;计量仪器及使用方法;试纸的使用;分液和萃取.
专题: 实验评价题.
分析: A.根据易分解的液体 存放在棕色细口瓶中,以及酸是腐蚀品;
存放在棕色细口瓶中,以及酸是腐蚀品;
B.铁离子水解生成胶体;
C.托盘天平的感量为0.1g;
D.为减少误差选择略大于所需浓硫酸体积且规格相近的量筒;
E.分液时有下层液体从分液漏斗的下端放出;
F.用广泛pH试纸测得的数值为整数.
解答: 解:A.实验室中浓硝酸应保存在棕色细口瓶中,并贴有如图所示标签,故A正确;
B.铁离子水解生成胶体,则向沸水中逐滴加入1mol•L﹣1的FeCl3溶液,并继续加热到液体呈透明的红褐色为止,得到胶体,故B正确;
C.托盘天平的感量为0.1g,所以不能称取5.85gNaCl,故C错误;
D.用10mL量筒量取5.6mL浓硫酸,故D错误;
E.用四氯化碳萃取碘水中的碘,有机层在下层,分液时有机层从分液漏斗的下端放出,故E正确;
F.用广泛pH试纸测得的数值为整数,故F错误;
故选ABE.
点评: 本题考查化学实验基本操作,题目难度中等,解答本题的关键是把握相关物质的性质,学习中注意积累.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
密闭容器中有如下反应:mA(g)+nB(g)⇌pC(g)达到平衡后,保持温度不变,将容器体积缩 小到原来的
小到原来的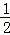 ,当达到新平衡时,C的浓度为原来的1.8倍.下列说法中正确的是()
,当达到新平衡时,C的浓度为原来的1.8倍.下列说法中正确的是()
A. m+n>p B. A的转化率降低
C. 平衡向正反应方向移动 D. C的质量分数增加
查看答案和解析>>
科目:高中化学 来源: 题型:
现有CO、CO2、O3(臭氧)三种气体,它们分别都含有1mol氧原子,则三种气体的物质的量之比为()
A. 1:1:1 B. 1:2:3 C. 3:2:1 D. 6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述正确的是()
A. 标准状况下,18gD2O中所含的质子数为10NA
B. 28gN2和CO的混合气体中含有的分子数为NA
C. 标准状况下,11.2LO2参加反应转移的电子数一定为2 NA
D. 5.6g铁与足量稀硫酸反应失去电子数为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述正确的是()
A. 氯气、活性炭都能使品红溶液褪色,它们的漂白原理相同
B. 滴加石蕊试液显红色的溶液:Fe3+、NH4+、I﹣可能大量共存
C. 某溶液中加入盐酸酸化的氯化钡产生白色沉淀,原溶液中一定含有SO42﹣
D. Fe(N03)2溶液中滴加少量稀硫酸会变黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与日常生活密切相关,下列说法错误的是()
A. 碘酒是指单质碘的乙醇溶液
B. 84消毒液的有效成分是NaClO
C. 浓硫酸可刻蚀石英制艺术品
D. 装饰材料释放的甲醛会造成污染
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是()
A. 含有最低价元素的化合物不一定具有很强的还原性
B. 元素的单质一定是由氧化或还原该元素的化合物制得
C. 阳离子只能得电子被还原,阴离子只能失电子被氧化
D. 在化学反应中,得电子越多的氧化剂,其氧化性就越强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学知识概括合理的是()
A. 酸性氧化物都是非金属氧化物
B. 一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
C. 丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
D. 熔融状态能导电的物质一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
用NaOH固体配制250mL 0.2mol•L﹣1 NaOH溶液.
(1)经计算需用NaOH固体 g
(2)配制该溶液用到的仪器有除托盘天平、烧杯、玻璃棒、量筒外,还有容量瓶;
(3)容量瓶上标有以下五项中的 (填序号)
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(4)配制溶液时,正确的操作顺序是(用字母表示,每个字母只能用一次) 并完成横线上的内容.
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用天平准确称取所需质量的NaOH,放入烧杯,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其充分溶解
C.将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液 .
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(5)在配制上述溶液实验中,下列操作引起结果(浓度)偏低的有 (填序号).
A.没有用蒸馏水洗烧杯2~3次,未将洗液移人容量瓶中
B.定容时,加水超过了刻度线,倒出一些再重新加水到刻度线
C.容量瓶刚用蒸馏水洗净,没有烘干.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com