


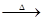 Pd��CO2����H2O��3�֣�
Pd��CO2����H2O��3�֣�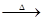 Pd��CO2����H2O��
Pd��CO2����H2O��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������������Ӧ���е������ɣ����Զ����û���Ӧ |
| B����������ǿ����˳��Ϊ KBrO3��KClO3��Cl2��Br2 |
| C����Ӧ���л�ԭ���������������ʵ���֮��Ϊ6��1 |
| D������lmol��ԭ����Ӧ���������õ����ӵ����ʵ���Ϊ2mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ��Al2O3��Fe2O3��SiO2�ȣ���ȡ��ͭ���̷���
��Al2O3��Fe2O3��SiO2�ȣ���ȡ��ͭ���̷��� ����������Kal��SO4��2
����������Kal��SO4��2 12H2O�ݵIJ����������£�
12H2O�ݵIJ����������£�

 ����Һ���еζ���MnO
����Һ���еζ���MnO ����ԭΪ
����ԭΪ ����
�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ʵ���У����漰�ĸ�������ԭ��Ӧ |
| B��ʵ���֤����ԭ�ԣ�H+��Fe2+��OH-��I- |
| C��ʵ��ڿ�֤���ܽ�ȣ�Fe(OH)3��Fe(OH)2 |
| D��ʵ����У���Ӧ�����ӷ���ʽ�ǣ�2Fe(OH)3+2I-+6H+=2Fe2++I2+6H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1molAl��������NaOH��Һ��Ӧ��ʧȥ�ĵ�����Ϊ3NA(NA��ʾ�����ӵ�����) |
| B��ԭ��صĸ�������������Ӧ�����ص�����������ԭ��Ӧ |
| C��Cu�ܱ�FeCl3��Һ��ʴ�������ӷ���ʽΪ��Cu+Fe3+=Cu2++Fe2+ |
| D��Na+��Ba2+��NO3����SO32��������������Һ������������ԭ��Ӧ�����ܴ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ۢ� | B���٢ڢܢ� | C���٢ڢۢ� | D��ֻ�Т٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2O2ֻ�������� |
| B��FeSO4Ϊ��ԭ�� |
| C����Ԫ�ر���ԭ |
| D��2 mol FeSO4������Ӧʱ����Ӧ�й���8 mol����ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��M����H+ | B��FeO42-���������� |
| C��ClO-�ڷ�Ӧ�б����� | D������1mol FeO42-ʱ��ת��1.5mol���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com