
 车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:
车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:| 物质 T/℃ | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
分析 (1)由表中数据可知,C、NO、E、F的化学计量数之比为(3.000-2.960):(0.10-0.020):0.040:0.040=1:2:1:1,反应中C被氧化,结合原子守恒可知,生成为N2与CO2;
(2)计算各气体的平衡浓度,代入平衡常数表达式计算;
(3)反应C+2NO?N2+CO2是一个气体体积不变的反应,而反应物只有一种,故加入NO气体,建立的平衡和原平衡为等效平衡;
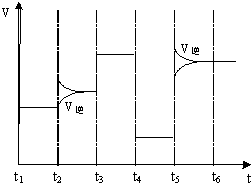
(4)t2、t3、t4、t5时改变某一种反应条件,所改变的条件均不同,可以判断每一时刻改变的条件.
解答 解:(1)由表中数据可知,C、NO、E、F的化学计量数之比为(3.000-2.960):(0.10-0.020):0.040:0.040=1:2:1:1,反应中C被氧化,结合原子守恒可知,生成为N2与CO2,且该反应为可逆反应,反应方程式为C+2NO?N2+CO2,
故答案为:C+2NO?N2+CO2;
(2)平衡时c(NO)=$\frac{0.020mol}{2L}$=0.010mol/L,c(N2)=c(CO2)=$\frac{0.040mol}{2L}$=0.020mol/L,故T1℃时该反应的平衡常数为K1=$\frac{0.020×0.020}{0.01{0}^{2}}$=4,
故答案为:4;
(3)反应C+2NO?N2+CO2是一个气体体积不变的反应,而反应物只有一种,故加入NO气体,建立的平衡和原平衡为等效平衡,原平衡中NO转化率为 $\frac{0.10-0.020}{0.10}$=80%,则达到新平衡时NO的转化率为80%,
故答案为:80%;
(4)改变的条件均不同,t5时刻,正逆反应速率均增大,且逆反应速率大于正反应速率,故t5时刻改变条件为升温,所以正反应为放热反应,升温平衡逆向移动,T1<T2,该反应△H<0,
故答案为:<.
点评 本题考查化学平衡图象、化学反应速率、影响化学平衡的因素,难度中等,是对知识的综合利用、注意基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 乙烷 | B. | 乙烯 | C. | 乙炔 | D. | 酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素b、c在同一周期 | |
| B. | 元素a、b、d各自最高和最低化合价的代数和均为0 | |
| C. | b的最高价氧化物对应的水化物酸性比d的弱 | |
| D. | 元素a、b、c不能存在于同一离子化合物中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
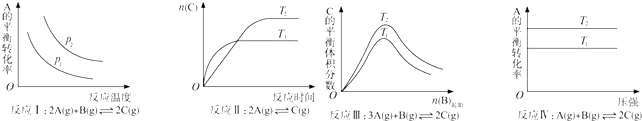
| A. | 反应Ⅰ:△H>0,P2>P1 | B. | 反应Ⅱ:△H<0,T1>T2 | ||
| C. | 反应Ⅲ:△H>0,T2<T1;或△H<0,T2>T1 | D. | 反应Ⅳ:△H<0,T2>T1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为18的氯原子可表示为18Cl | |
| B. | 某金属阳离子的结构示意图为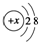 ,其与Cl-形成的化合物都是离子化合物 ,其与Cl-形成的化合物都是离子化合物 | |
| C. | 二硫化碳的电子式为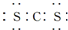 | |
| D. | 17.4g熔融K2SO4与7.8 g熔融Na2O2中阴离子数目相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH固体 | B. | 同浓度的醋酸溶液 | ||
| C. | NH4Cl固体 | D. | CH3COONa固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com