
| A.若X是固体,则t1时一定是增大了容器的压强 |
| B.若X是气体,则t2时可能是增大了容器的压强 |
| C.若X是固体,则t1时可能是增大了X的质量 |
| D.t2时不可能是减小容器压强;若采用了降温措施,则该反应的正反应方向△H<0 |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:不详 题型:单选题
 N2O4(气)(正反应为放热反应)在测定NO2的相对分子质量时,下列条件中较为适宜的是( )
N2O4(气)(正反应为放热反应)在测定NO2的相对分子质量时,下列条件中较为适宜的是( )| A.温度130℃、压强3.03×105Pa |
| B.温度25℃、压强1.01×105Pa |
| C.温度130℃、压强5.05×104Pa |
| D.温度0℃、压强5.05×104Pa |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g) ΔH<0的下列条件后,下列叙述中错误的是( )
2NH3(g) ΔH<0的下列条件后,下列叙述中错误的是( )| A.加入催化剂,v正、v逆都发生变化,且变化的倍数相等 |
| B.增大压强,v正、v逆都增大,v正增大的倍数大于v逆增大的倍数 |
| C.降低温度,v正、v逆都减小,且v正减小的倍数小于v逆减小的倍数 |
| D.加入氩气,v正、v逆都增大,且v正增大的倍数大于v逆增大的倍数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
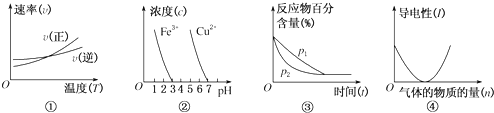
| A.根据图①可判断反应的△H<0 |
| B.根据图②,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 |
| C.图③可表示压强(p)对反应2A(g)+2B(g)?3C(g)+D(s)的影响 |
| D.图④可表示向醋酸溶液中通入氨气时,溶液导电性随氨气量的变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通入水蒸气 | B.缩小容器体积 |
| C.分离出CO2 | D.升高温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 |
| D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.催化剂是通过降低反应所需的活化能来增大反应速率的 |
| B.对于有气体参加的反应,压强增大,单位体积内的活化分子数增多,发生有效碰撞的机会增多,反应速率加快 |
| C.发生碰撞的分子只要具有足够的能量,就能够发生有效碰撞 |
| D.光、电磁波、超声波等因素会对反应速率产生影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.水 | B.铜粉 | C.CH3COONa | D.NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com