
| A、Cl2、O2 |
| B、SO2、NO |
| C、NO、NO2 |
| D、O2、SO2 |


 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:
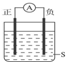
| A、正极Cu,负极Zn,S为稀H2SO4 |
| B、正极Zn,负极Cu,S为CuSO4溶液 |
| C、正极Ag,负极Zn,S为AgNO3溶液 |
| D、正极Fe,负极Cu,S为AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 电池 | 电解池 | |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3mol Pb | 生成1mol Al2O3 |
| C | 正极:PbO2+4H++2e-=Pb2++2H2O | 阳极:2Al+3H2O-6e-=Al2O3+6H+ |
| D | Pb电极反应质量不变 | Pb电极反应质量不变 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Fe(NO3)3溶液中加入过量的HI溶液:2NO3-+8H++6I-═3I2+2NO↑+4H2O |
| B、硫酸溶液中加入足量氢氧化钡溶液:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| C、亚硫酰氯(SOCl2)剧烈水解生成两种酸:SOCl2+2H2O═H2SO3+2H++2Cl- |
| D、将碳与足量的浓硫酸共热反应后的气体混合物,通入过量氢氧化钠溶液中:CO2+SO2+4OH-═SO32-+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
| B、1.0mol?L-1 KNO3溶液:H+、Fe2+、Cl-、SO42- | ||
| C、含有0.1mol?L-1 Ca2+溶液:Na+、K+、CO32-、Cl- | ||
| D、澄清透明的溶液:Na+、K+、MnO4-、[Al(OH)4]- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+、Fe3+、NO3-、I- |
| B、K+、Na+、Cl-、SO42- |
| C、Mg2+、Ca2+、CO32-、AlO2- |
| D、K+、NH4+、SO42-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、微粒半径:F->O2->Na+>Li+ |
| B、电负性Cl>C,酸性:HClO4>H2CO3 |
| C、分子中的键角:CH4>H2O>CO2 |
| D、稳定性:LiCl<NaCl<KCl<RbCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一个氮原子的质量就是氮的相对原子质量 |
| B、一个碳原子的质量约为1.99×10-23g |
| C、氧气的摩尔质量在数值上等于它们的相对分子质量 |
| D、氢氧化钠的摩尔质量是40g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com