
【题目】某研究小组为探究SO2和Fe(NO3)3溶液的反应的实质。设计了如下图所示装置进行实验.
已知:1.0 mol/L的Fe(NO3)3溶液的pH=1。

请回答:
(1)装置A中用于添加浓硫酸的仪器名称为__________________。
(2)实验前鼓入N2的目的是________________________________。
(3)装置B中产生了白色沉淀,其成分是________,说明SO2具有________性。
(4)分析B中产生白色沉淀的原因。
观点1:SO2与Fe3+反应;
观点2:在酸性条件下SO2与NO3-反应;
①若观点1正确,除产生沉淀外,还应观察到的现象是_________________。
②按观点2,装置B中反应的离子方程式是______________________________,
③有人认为,如将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择的最佳试剂是(填序号)_____。
A.1 mol/L稀硝酸 |
B.1.5 mol/L Fe(NO3)2溶液 |
C.6.0 mol/L NaNO3溶液和0.2 mol/L盐酸等体积混合的溶液 |
D.3.0 mol/L NaNO3溶液和0.1mol/L硫酸等体积混合的溶液 |
【答案】分液漏斗 排净装置中的空气,防止溶液中SO2被空气中的O2氧化而干扰实验 BaSO4 还原 静置一段时间后,溶液由棕黄色变为浅绿色 3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+或3SO2+2NO3-+2H2O=3SO42-+2NO+4H+;Ba2++SO42- = BaSO4↓ C
【解析】
本题以二氧化硫为载体考查了性质实验方案设计,明确实验原理是解本题关键,根据物质的性质进行假设,然后采用验证的方法进行探究,结合氧化还原反应分析解答。
(1)装置A中用于添加浓硫酸,为滴加液体的仪器,该仪器名称为分液漏斗,故答案为:分液漏斗;
(2)氧气、硝酸根离子都能将二氧化硫氧化,所以如果装置中含有氧气,会干扰实验,所以排入氮气的目的是排净空气防止干扰实验,故答案为:排净装置中的空气,防止溶液中SO2被空气中的O2氧化而干扰实验;
(3)二氧化硫具有还原性,酸性条件下,能被硝酸根离子氧化生成硫酸根离子,硫酸根离子和钡离子反应生成硫酸钡白色沉淀,故答案为:BaSO4;还原;
(4)①若观点1正确,二氧化硫和铁离子发生氧化还原反应生成硫酸根离子和亚铁离子,硫酸根离子和钡离子反应生成白色沉淀,溶液由黄色变为浅绿色,所以除产生沉淀外,还应观察到的现象是静置一段时间后,溶液由棕黄色变为浅绿色,故答案为:静置一段时间后,溶液由棕黄色变为浅绿色;
②按观点2,酸性条件下,硝酸根离子和二氧化硫发生氧化还原反应生成硫酸根离子和NO,硫酸根离子和钡离子反应生成硫酸钡白色沉淀,离子反应方程式为:3SO2+2NO3-+3Ba2++2H2O═3BaSO4↓+2NO↑+4H+或3SO2+2NO3-+2H2O═3SO42-+2NO↑+4H+、Ba2++SO42-═BaSO4↓,故答案为:3SO2+2NO3-+3Ba2++2H2O═3BaSO4↓+2NO↑+4H+或3SO2+2NO3-+2H2O═3SO42-+2NO↑+4H+、Ba2++SO42-═BaSO4↓;
③乙同学的观点是:酸性条件下,二氧化硫和硝酸根离子发生氧化还原反应,只要溶液中硝酸根离子浓度不变即,实验中c(NO3-)=3mol/L,则可用6.0molL-1NaNO3和0.2molL-1盐酸等体积混合的溶液代替,故答案为:C。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】已知:①从石油中获得是目前工业上生产A的主要途径,A的产量通常用来衡量一个国家的石油化工发展水平;②2CH3CHO+O2![]() 2CH3COOH。
2CH3COOH。
现以A为主要原料合成乙酸乙酯,其合成路线如图所示:

回答下列问题:
(1)写出A的结构简式:___。
(2)B、D分子中的官能团名称分别是___、___。
(3)写出下列反应的反应类型:①___,②___,④___。
(4)写出下列反应的化学方程式:
①___。
②___。
④___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 是具有相同电子层结构的短周期元素形成的简单离子。下列叙述正确的是
是具有相同电子层结构的短周期元素形成的简单离子。下列叙述正确的是
A.原子半径: C>D>A>BB.原子序数: b>a>d>c
C.离子半径: D>C>A>BD.单质还原性: A>B>C>D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率
4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率![]() x
x
A. ![]() (O2) = 0.01mol·(L·s) –1 B.
(O2) = 0.01mol·(L·s) –1 B. ![]() (NO) = 0.008mol·(L·s) –1
(NO) = 0.008mol·(L·s) –1
C. ![]() (H2O) = 0.006mol·(L·s) –1 D.
(H2O) = 0.006mol·(L·s) –1 D. ![]() (NH3) = 0.002mol·(L·s) –1
(NH3) = 0.002mol·(L·s) –1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]![]() 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是________________________________________。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________、___________。
③为防止倒吸,停止实验时应进行的操作是_____________________________。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近有科学家发现正丁烷(![]() )脱氢或不完全氧化也可制得1,3-丁二烯(
)脱氢或不完全氧化也可制得1,3-丁二烯(![]() ),已知热化学方程式如下:( )
),已知热化学方程式如下:( )
①![]() =
=![]()
![]()
②![]() =
=![]()
![]()
③![]() =
=![]()
![]()
下列说法正确的是( )
A.由②可知,正丁烷(![]() )的燃烧热为
)的燃烧热为![]()
B.由①和②可推知:![]() =
=![]()
![]()
C.![]() =
=![]()
![]()
D.由①和②可知,同质量的正丁烷(![]() )转变为1,3-丁二烯(
)转变为1,3-丁二烯(![]() )所需要的能量相同
)所需要的能量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,向A和B中都充人2molX和2molY,起始VA=0.8a L,VB=a L保持温度不变,在有催化剂的条件下,两容器中各自发生下列反应:X(g)+Y(g)![]() 2Z(g)+W(g)达到平衡时,VA=0.9a L,则下列说法错误的是 ( )
2Z(g)+W(g)达到平衡时,VA=0.9a L,则下列说法错误的是 ( )
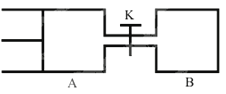
A. 两容器中达到平衡的时间A<B
B. 打开K达到新平衡后,升高B容器温度,A容器体积相比原平衡状态时一定增大
C. A容器中X的转化率为25%,且比B容器中的X的转化率小
D. 打开K一段时间达平衡时,A的体积为0.8a L(连通管中的气体体积不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置测定中和热的实验步骤如下:

①用量筒量取50mL0.25mol·L-1硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL0.55mol·L-1NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是____________。
(2)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ·mol-1)___________。
(3)倒入NaOH溶液的正确操作是__________(从下列选项中选出)。
A.沿玻璃棒缓慢倒入B.分三次少量倒入C.一次迅速倒入
(4)实验数据如表:
①请填写下表中的空白:
起始温度t1℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | |||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | _____ |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55mol·L-1NaOH溶液和0.25mol·L-1硫酸溶液的密度都是1g·cm-3,中和后生成溶液的比热容c=4.18J·g-1·℃-1。则中和热ΔH=________(取小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符合的是

A. 图甲表示对某化学平衡体系改变温度后反应速率随时间的变化
B. 图乙表示反应物断键吸收的能量大于生成物成键放出的能量
C. 图丙表示0.1 mol·L-1NaOH溶液滴定20 mL 0.1 mol·L-1硫酸时溶液pH的变化
D. 图丁表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化情况
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com