
| A、84.7% |
| B、72.6% |
| C、12.1% |
| D、6.05% |
| 1 |
| 7 |


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
| H2(g) | N2(g) | NH3(g) | |
| 1mol分子中的化学键形成时要释放出的能量/kJ | 436 | 946 | a |
A、如图可表示合成氨过程中的能量变化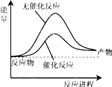 |
| B、a的数值为1173 |
| C、Q的数值为92 |
| D、其它条件相同,反应使用催化剂时释放出的能量大于无催化剂时释放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH的摩尔质量为40g |
| B、64g SO2中含有1mol O2 |
| C、1mol N2的体积为22.4L |
| D、0.5mol CO2约含有3.01×1023个CO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、保鲜膜、一次性食品袋的主要成分是聚氯乙烯 |
| B、乙烯、聚乙烯都能使溴水褪色 |
| C、利用可降解的“玉米塑料”替代一次性饭盒,可减少白色污染 |
| D、人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用次氯酸钙溶液吸收过量二氧化碳:ClO-+CO2+H2O=HCO3-+HClO |
| B、向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| C、2.24L(标况下)Cl2通入100mL1mol/LFeBr3溶液中:Cl2+2Br-=2Cl-+Br2 |
| D、在NaOH溶液中通入过量二氧化碳:CO2+2OH-=CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ).下列有关说法不正确的是( )
).下列有关说法不正确的是( )| A、羊毛的主要成分属于蛋白质 |
| B、涤纶属于天然高分子化合物 |
| C、合成涤纶的单体之一可以是HOCH2CH2OH |
| D、可用灼烧的方法区别羊毛和涤纶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 a.肼又叫联氨,其化学式为N2H4,为无色中性液体,熔点275K,沸点386.5K,1g肼彻底燃烧时放出19.5kJ的热量(通常状况下测定,产物中有氮气),是一种清洁的能源物质.古典的Rasching法制备肼是以次氯酸钠和足量的氨反应,获得肼的稀溶液,该溶液中还含有氯离子,回答:
a.肼又叫联氨,其化学式为N2H4,为无色中性液体,熔点275K,沸点386.5K,1g肼彻底燃烧时放出19.5kJ的热量(通常状况下测定,产物中有氮气),是一种清洁的能源物质.古典的Rasching法制备肼是以次氯酸钠和足量的氨反应,获得肼的稀溶液,该溶液中还含有氯离子,回答:| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com