
CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
(1)下列关于CO2的说法正确的是(填序号)_________。
①减少化石燃料的使用,充分利用太阳能、风能等清洁能源可有效降低大气中CO2的含量
②植树造林,增大植被面积可以有效降低大气中CO2的含量
③二氧化硫、氮氧化物、二氧化碳、悬浮微粒的含量都是空气质量日报的内容
④空气中CO2的含量过高会导致酸雨的形成
(2)下列措施不能减少二氧化碳排放的是(填序号) _________。
①利用太阳能制氢
②关停小火电企业
③举行“地球一小时”熄灯活动
④推广使用煤液化技术
(3)下列反应不产生温室气体的是(填序号)_________。
①用纯碱制玻璃 ②用煤炭作燃料
③用铁矿石炼铁 ④用氨制碳酸铵
(4)目前,关于二氧化碳是否为大气污染物有不同的观点。认为“二氧化碳不是大气污染物”的理由是(填序号)_________。
①二氧化碳是重要的化工原料
②二氧化碳是植物光合作用的必备原料
③二氧化碳是无色、无味、无毒的气体
④除二氧化碳以外,甲烷、一氧化二氮等也是温室气体
(1)①、② (2)④ (3)④ (4)②③
【解析】(1)①可以直接减少CO2的产生,正确;②植树造林,增大植被面积能够增强植物的光合作用,是吸收CO2的重要途径,正确;③二氧化碳虽然会造成温室效应,但对空气质量影响不大,故不列入污染物;④空气中的SO2含量过高是酸雨形成的主要原因,本题选①、②。
(2)利用太阳能制氢,减少了化石燃料的使用,同时也减少了CO2的排放,①项符合;火力发电消耗大量的煤炭资源,同时会排放出CO2及有害气体,关停小火电企业,有利于节能减排,②项符合;举行“地球一小时”熄灯活动能有效地节约电能,可以减少CO2的排放,③项符合; 煤液化技术,提高了煤的利用率,但不能减少CO2的排放,④项不符合,选④。
(3)①制玻璃的反应为:Na2CO3+SiO2 Na2SiO3+CO2↑;②煤炭燃烧可产生CO2气体;③铁矿石与C或CO反应可生成CO2;这三项均生成CO2,即产生温室气体。④NH3与CO2反应生成(NH4)2CO3,没有产生CO2,选④。
Na2SiO3+CO2↑;②煤炭燃烧可产生CO2气体;③铁矿石与C或CO反应可生成CO2;这三项均生成CO2,即产生温室气体。④NH3与CO2反应生成(NH4)2CO3,没有产生CO2,选④。
(4)化工原料不一定不是大气污染物,还有其他气体能引起温室效应不能说明二氧化碳不是大气污染物,②③正确。


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源:2014年化学高考总复习课时演练 5-3化学键练习卷(解析版) 题型:选择题
下列说法中正确的是( )
A.在离子化合物NaOH中,既存在离子键,也存在非极性共价键
B.非极性键只存在于双原子的单质分子(如Cl2)中
C.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键
D.NH4HCO3加热时闻到刺激性的气味,在此过程中,只有共价键被破坏
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 4-4氮及其重要化合物练习卷(解析版) 题型:选择题
2011年中国汽车销量增长幅度很大,同时也带来了空气污染。汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是
( )

A.反应中NO为氧化剂,N2为氧化产物
B.汽车尾气的主要污染成分包括CO、NO和N2
C.NO和O2必须在催化剂表面才能反应
D.催化转化总反应为2NO+O2+4CO 4CO2+N2
4CO2+N2
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 4-2富集在海水中的元素-氯练习卷(解析版) 题型:选择题
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示。有关说法不正确的是( )
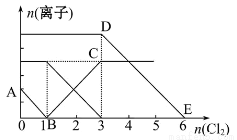
A.线段BC代表Fe3+物质的量的变化情况
B.原混合溶液中c(FeBr2)=6 mol/L
C.当通入Cl2 2 mol时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.原溶液中n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 4-2富集在海水中的元素-氯练习卷(解析版) 题型:选择题
已知常温下氯酸钾与浓盐酸反应放出氯气,现按如图所示装置进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是( )

查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 4-1无机非金属材料的主角-硅练习卷(解析版) 题型:选择题
将足量CO2通入下列各溶液中,所含离子还能大量共存的是( )
A.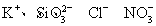
B.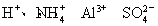
C.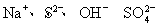
D.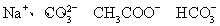
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 3-3铁及其重要化合物练习卷(解析版) 题型:实验题
某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:

【探究一】设计如图所示装置进行“铁与水反应”的实验。
(1)硬质玻璃管中发生反应的化学方程式为______________________________。
(2)反应前A中投放碎瓷片的目的是____________________________________。
(3)装置E中的现象是________________________________________________。
【探究二】设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于_______后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分(选填序号,下同)为_______;若溶液未变红色,推断硬质玻璃管B中固体物质的成分为_______。
①一定有Fe3O4 ②一定有Fe
③只有Fe3O4 ④只有Fe
(6)另一份用_______(填仪器名称)加入_______,可以证明溶液中存在Fe2+。
【探究三】设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(7)试剂b的化学式是_______。
(8)计算反应后B装置中铁元素的质量分数为_______。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 3-2铝及其重要化合物练习卷(解析版) 题型:选择题
把4.6 g钠放入100 mL 0.1 mol/L AlCl3溶液中,待其充分反应后(水蒸发不计),下列叙述中错误的是( )
A.Cl-浓度不变
B.溶液仍有浑浊
C.溶液中几乎不存在Al3+
D.溶液中存在最多的离子是Na+
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 2-2离子反应练习卷(解析版) 题型:选择题
实验室需配制一种仅含四种离子(不包括水电离出的离子)的无色混合溶液,且在混合溶液中四种离子的物质的量浓度均为1 mol/L。下面四个选项中能达到此目的的是( )
A.Na+、K+、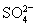 、Cl- B.Cu2+、K+、
、Cl- B.Cu2+、K+、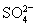 、
、
C.H+、K+、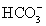 、Cl- D.Mg2+、Na+、Cl-、
、Cl- D.Mg2+、Na+、Cl-、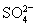
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com