
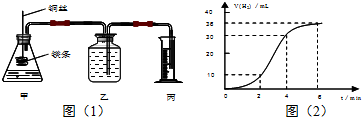
分析 (1)①先根据图2找出2、4、6min时刻时的氢气体积的变化量,再找出2、4、6min时刻时的速率与时间的关系,然后用平滑曲线描绘图象;
②根据该反应的反应热及溶液中氢离子的浓度判断;
(2)①原因Ⅱ:先确定Cl-对反应没有影响再猜测硫酸根离子的作用;
原因Ⅴ:根据原因Ⅳ提出与原因Ⅳ相反的观点;
②根据a、b对比实验中的现象判断原因Ⅲ.
解答 解:(1)①2、4、6min时刻时氢气体积的分别为10 mL、20mL、36mL,其平均反应速率分别为5 mL/min、7.5mL/min、6mL/min,然后标出速率与时间图象为: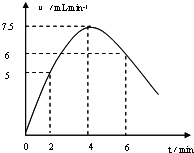 ,
,
故答案为: ;
;
②该反应是放热反应,随着反应的进行,放出的热量越多,溶液的温度越高,反应速率越大;随着反应的进行,溶液中氢离子的浓度逐渐减小,浓度越小,反应速率越小.
故答案为:镁和盐酸反应是放热反应,随着反应体系温度升高,反应速率增大;4min后由于溶液中H+浓度降低,所以导致反应速率减小;
(2)①根据原因Ⅰ结合题意,提出与原因Ⅰ相反的观点,原因Ⅱ为:Cl-对反应没有影响,而SO42-对反应具有阻碍作用,
故答案为:Cl-对反应没有影响,而SO42-对反应具有阻碍作用;
根据原因Ⅳ结合题意,提出与原因Ⅳ相反的观点,原因Ⅴ为:Cl-、SO42-均对反应具有阻碍作用,但Cl-影响更小(或SO42-影响更大),
故答案为:Cl-、SO42-均对反应具有阻碍作用,但Cl-影响更小(或SO42-影响更大).
②a中原来时快有硫酸根离子,后加入氯离子,如果氯离子有促进作用,那么反应速率就比未加时快,以此证明原因Ⅲ是正确的;
b中中原来时快有氯离子,后加入硫酸根离子,如果硫酸根离子有阻碍作用,那么反应速率比未加时慢,以此说明因Ⅲ是正确的,
故答案为:反应速率加快;反应速率减慢.
点评 本题考查了影响化学反应速率的因素,题目难度中等,影响化学反应速率的外界条件有:温度、浓度、压强、催化剂等,试题知识点较多、综合性较强,充分考查了学生得到分析能力及化学实验能力.


科目:高中化学 来源: 题型:解答题
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 四 | ⑧ | ⑨ |
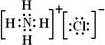 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
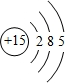 ,E的最高价含氧酸的化学式HClO4.
,E的最高价含氧酸的化学式HClO4. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 它在地壳中储量丰富,是人体不可缺少的微量元素之一.其单质为银白色固体,是工农业生产中不可或缺的金属材料,常用于机械制备、建筑等行业 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.
已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
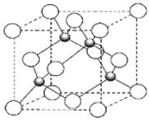 X、Z、Q、R、T为前四周期元素,且原子序数依次增大.X和Q属同族元素,X和R可形成化合物XR4;R2为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;T2+的3d 轨道中有5个电子.请回答下列问题:
X、Z、Q、R、T为前四周期元素,且原子序数依次增大.X和Q属同族元素,X和R可形成化合物XR4;R2为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;T2+的3d 轨道中有5个电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝是白色胶状沉淀,能凝聚水中的悬浮物,但不能吸附色素 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大题水冲洗,然后涂上硼酸 | |
| C. | 氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却 | |
| D. | 酒精灯着火时可用水扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场 | |
| B. | 氢气在盛有氯气的集气瓶中燃烧,瓶口有白烟产生 | |
| C. | 氯气能与铁反应,液氯不宜贮存在钢瓶中 | |
| D. | 工业上以氯气和澄清石灰水为原料制造漂白粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com