
【题目】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
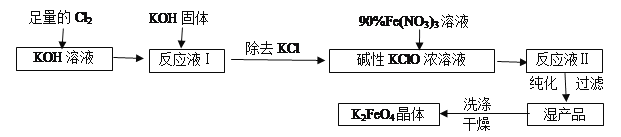
请回答下列问题:
(1)写出向KOH溶液中通入足量Cl2发生反应的离子方程式___________。
(2)在溶液Ⅰ中加入KOH固体的目的是________(填编号)。
A.为下一步反应提供碱性的环境
B.使KClO3转化为KClO
C.与溶液Ⅰ中过量的Cl2继续反应,生成更多的KClO
D.KOH固体溶解时会放出较多的热量,有利于提高反应速率
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3,KCl,则反应③中发生的离子反应方程式为________。每制得59.4克K2FeO4,理论上消耗氧化剂的物质的量为________mol。
(4)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式: FeO42-+ H2O= Fe(OH)3(胶体)+ O2↑+ OH-。___________
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图所示。电解过程中阳极的电极反应式为_____________。
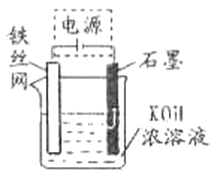
【答案】 2OH-+Cl2=ClO-+Cl-+H2O AC 2Fe3++3C1O-+10OH-=2FeO42-+3Cl-+5H2O 0.45 4FeO42-+10H2O![]() 4Fe(OH)3(胶体)+3O2↑+8OH- Fe+8OH--6e-=FeO42-+4H2O
4Fe(OH)3(胶体)+3O2↑+8OH- Fe+8OH--6e-=FeO42-+4H2O
【解析】足量Cl2通入和KOH溶液中,温度低时发生反应Cl2+2OH-=Cl-+ClO-+H2O,Cl2+H2O=H++Cl-+HClO,向溶液I中加入KOH,使氯气完全反应,且将溶液转化为碱性溶液,只有碱性条件下次氯酸根离子才能和铁离子发生氧化还原反应生成高铁酸根离子,除去KCl得到碱性的KClO浓溶液,向碱性的KClO浓溶液中加入90%的Fe(NO3)3溶液,发生反应2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,得到溶液II,纯化得到湿产品,将湿产品洗涤、干燥得到晶体K2FeO4,
(1)KOH溶液和足量Cl2发生反应生成KCl、KClO和H2O,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,Cl2+H2O=H++Cl-+HClO;(2)KOH和氯气反应生成KClO,除去未反应的氯气,且只有碱性条件下,铁离子才能和次氯酸根离子发生氧化还原反应生成高铁酸根离子,所以加入KOH的目的是除去氯气且使溶液为碱性,故选AC;(3)反应③中铁离子和次氯酸根粒子发生氧化还原反应生成高铁酸根离子,离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;n(K2FeO4)=59.4g/198g·mol-1=0.3mol,根据2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O知,氧化剂的物质的量=0.3mol×3/2=0.45mol。(4)该反应中Fe元素化合价由+6价变为+3价、O元素化合价由-2价变为0价,其转移电子数为6,根据转移电子相等、电荷守恒配平方程式为4FeO42-+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-,故系数为:4;10;4;3;8。(5)在碱性条件下,铁失去电子被氧化,阳极的电极反应式为Fe+8OH--6e-=FeO42-+4H2O。


科目:高中化学 来源: 题型:
【题目】利用碳纳米管能够吸附氢气,设计一种新型二次电池,其装置如图所示。关于该电池的叙述不正确的是( )
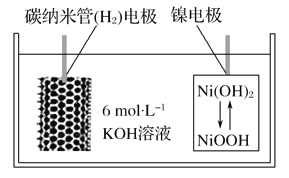
A. 电池放电时K+移向正极
B. 电池放电时负极反应为:H2-2e-+2OH-===2H2O
C. 电池充电时镍电极上NiOOH转化为Ni(OH)2
D. 电池充电时碳纳米管电极与电源的负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取、净化并收集氯气涉及以下几个主要阶段:
![]()
![]()
![]()
![]() 尾气处理
尾气处理
(1)写出实验室制取氯气的离子方程式____________________________,NA表示阿伏加德罗常数的值,若有4 mol的HCl被氧化,则转移的电子总数为______;将足量的MnO2投入含2 mol HCl的浓盐酸中,充分加热,可生成的Cl2________(填“>”“=”或“<”)0.5 mol。
(2)现有3种试剂可供选择:A.饱和食盐水 B.浓硫酸 C.NaOH溶液,则Y溶液应选用________(填字母),X溶液的作用是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辣椒素是辣椒的活性成分,可在口腔中产生灼烧感,能够起到降血压和胆固醇的功效,进而在很大程度上预防心脏病,也能缓解肌肉关节疼痛。辣椒素酯类化合物的结构可以表示为:
 (R为烃基)
(R为烃基)
其中一种辣椒素酯类化合物J的合成路线如下:
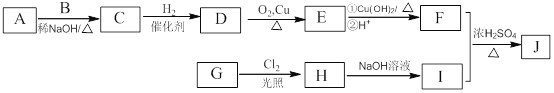
已知:
①A、B和E为同系物,其中B的相对分子质量为44,A和B核磁共振氢谱显示都有两组峰;
②化合物J的分子式为C15H22O4;
③
回答下列问题:
(1)G所含官能团的名称为 。
(2)由A和B生成C的化学方程式为 。
(3)由C生成D的反应类型为 ,D的化学名称为 。
(4)由H生成I的化学方程式为 。
(5)J的结构简式为 。
(6)G的同分异构体中,苯环上的一氯代物只有一种的共有 种(不含立体异构),核磁共振氢谱显示2组峰的是 (写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组对以下三种品牌牙膏中摩擦剂成分进行调查,结果如下表:
牙膏品牌 | A儿童牙膏 | B防臭牙膏 | C透明牙膏 |
摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(1)上述三种摩擦剂成分中属于酸性氧化物的是________(填化学式,下同);既能与强酸反应又能与强碱反应的是________。
(2)A儿童牙膏中摩擦剂成分与NaOH溶液反应的离子方程式是______________________________。
(3)从摩擦剂成分考虑,向B防臭牙膏样品中滴加少量稀盐酸,可观察到的现象是______________________________________,该反应的化学方程式为_______________________。
(4)C透明牙膏摩擦剂成分SiO2是工业制备晶体硅的原料,其反应原理是_______________(用化学反应方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向l0mL0.1mol/L的HR溶液中逐渐滴入0.lmol/L的NH3·H2O 溶液,所得溶液pH及导电性变化如图。下列分析不正确的是
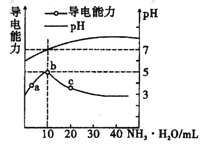
A. ab点导电能力增强,说明HR为弱酸
B. b点溶液,c(NH3H2O)=c(R-)+c(H+)-c(OH-)
C. c点溶液,存在c(NH4+)>c(R-)>c(OH-)>c(H+)
D. 常温下,HR和NH3H2O的电离平衡常数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积0.1 mol·L-1一元弱酸HA溶液中逐滴加入等浓度的NaOH溶液,溶液中pH与pOH[pOH=-1gc(OH-)]的变化关系如图所示。 下列说法错误的是
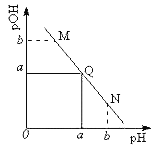
A. 此温度下,水的离子积常数为1.0×10-2a
B. M、N两点所示的溶液中,水的电离程度相同
C. Q点消耗的NaOH溶液的体积等于HA溶液的体积
D. N点溶液加水稀释,![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)当SO2、SO3的分子个数之比为1∶1时,原子总数之比为________,质量之比为________。
(2)中和含0.2 mol HCl的稀盐酸,需NaOH的质量为________g。
(3)将5 mol·L-1的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO![]() 的物质的量浓度是______ mol·L-1。
的物质的量浓度是______ mol·L-1。
(4)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中的SO![]() 都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为________。
都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于反应速率、反应限度的下列说法中正确的是( )
A.其他条件不变时,升高温度,只有吸热反应,反应速率加快
B.化学反应的限度是不可改变的
C.化学反应达到反应限度时,反应物的浓度与生成物的浓度相等
D.化学反应达到反应限度时,同一物质的正反应速率与逆反应速率相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com