
【题目】金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)①铜或铜盐的焰色反应为绿色,下列有关原理分析的叙述正确的是___ (填字母)。
A. 电子从基态跃迁到较高的激发态 B. 电子从较高的激发态跃迁到基态
C. 焰色反应的光谱属于吸收光谱 D. 焰色反应的光谱属于发射光谱
②碘、铜两种元素的电负性如表:
元素 | I | Cu |
电负性 | 2.5 | 1.9 |
CuI属于_______(填“共价”或“离子”)化合物。
(2)氯化铁溶液用于检验食用香精乙酰乙酯时,会生成紫色配合物,其配离子结构如图所示。
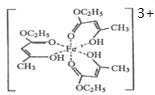
①此配合物中,基态铁离子的价电子排布图为________________。
②此配合物中碳原子的杂化轨道类型有________________。
③此配离子中含有的化学键有____________(填字母)。
A.σ键 B.π键 C.极性键 D.非极性键 E. 配位键 F. 氢键 G.离子键
(3)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是_____________。
(4)治疗铅中毒可滴注依地酸(别名EDTA,结构如下面左图)钠钙,使Pb2+转化为依地酸铅盐。下列说法正确的是_________(填标号)
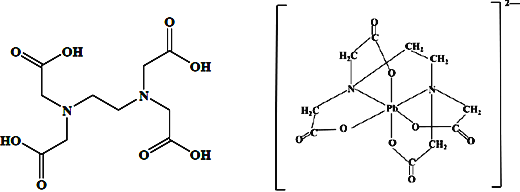
A.形成依地酸铅离子所需n(Pb2+):n(EDTA)=1:4
B.依地酸中各元素的电负性从大到小的顺序为O>N>C>H
C.依地酸铅盐中含有离子键和配位键
(5)AlCl3是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态还是气态,一个分子中的氯原子与另外一个铝原子形成配位键,因此以二聚体Al2Cl6的形式存在,写出Al2Cl6的结构式_______(用→标出配位键)。
【答案】BD 共价 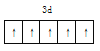 sp2、sp3 ABCDE 异硫氰酸 BC
sp2、sp3 ABCDE 异硫氰酸 BC 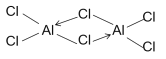
【解析】
焰色反应时,电子由较高能级跃迁到较低能级时,以光的形式释放能量。
(1)①铜或铜盐的焰色反应为绿色。焰色反应时,电子由较高能级跃迁到较低能级时,以光的形式释放能量,故A错误、B正确;焰色反应的光谱属于发射光谱,故C错误、D正确;故选BD;② CuI中2种元素的电负性数值之差2.5-1.9=0.6<1.7,属共价化合物;
(2)①铁元素是26号元素,其原子核外有26个电子,铁原子失去3个电子变成铁离子,其价电子排布式为:3d5,价电子排布图为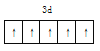 ;②甲基和乙基上的碳原子采用sp3杂化,碳碳双键两端的碳原子采用sp2杂化; ③同种非金属元素之间存在非极性键,不同非金属元素之间存在极性键,含有孤电子对的原子和含有空轨道的原子之间可以形成配位键,共价单键为σ键,共价双键中含有一个σ键和一个π键,所以该化合物中碳原子之间存在非极性共价键,碳和氧原子或氢原子之间存在极性共价键,铁离子和氧原子之间存在配位键,则该化合物中含有配位键、极性键、非极性键、σ键和π键,故选ABCDE;
;②甲基和乙基上的碳原子采用sp3杂化,碳碳双键两端的碳原子采用sp2杂化; ③同种非金属元素之间存在非极性键,不同非金属元素之间存在极性键,含有孤电子对的原子和含有空轨道的原子之间可以形成配位键,共价单键为σ键,共价双键中含有一个σ键和一个π键,所以该化合物中碳原子之间存在非极性共价键,碳和氧原子或氢原子之间存在极性共价键,铁离子和氧原子之间存在配位键,则该化合物中含有配位键、极性键、非极性键、σ键和π键,故选ABCDE;
(3)由于异硫氰酸分子间可形成氢键,而硫氰酸分子间不能形成氢键,所以硫氰酸的沸点低于异硫氰酸;
(4)根据依地酸铅离子的结构和依地酸的结构,结合氮原子守恒,n(Pb2+):n(EDTA)=1:1,A项错误;依地酸中含有元素H、C、N、O,其电负性从大到小的顺序为O>N>C>H,B正确;依地酸铅盐中含有离子键(依地酸根离子与铅离子之间)和配位键(依地酸根中氮原子与Pb2+之间),C选项正确;正确答案选BC。
(5)AlCl3是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态还是气态,一个分子中的氯原子与另外一个铝原子形成配位键,因此以二聚体Al2Cl6的形式存在,依据以上信息判断AlCl3晶体的结构属于分子晶体,Al2Cl6的结构式为: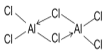


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】如图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。下列判断不正确的是( )
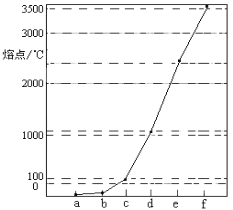
A. 图中对应的e、f单质晶体熔化时克服的是共价键
B. d单质对应元素的电子排布式:1s22s22p63s23p2
C. b元素形成的最高价含氧酸易与水分子之间形成氢键
D. 单质a、b、f对应的元素以原子个数比1∶1∶1形成的最简单分子中含2个σ键和2个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某原电池的装置图。其电池的总反应是:2Ag+(aq) + Cu(s) = Cu2+(aq) + 2Ag(s)。请回答以下问题:
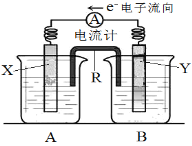
(1)R的名称是__________,R中的阳离子移向________(填“A”或“B”)中的溶液。
(2)电极Y的材料是______________,B中的电解质溶液是________________。
(3)X为原电池的______(填“正”或“负”)极,其电极反应式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
(1)根据如图提供的信息,写出该反应的热化学方程式____________________________,下图的曲线中________(填“a” 或“b”)表示加入铁触媒(催化剂)的能量变化曲线。
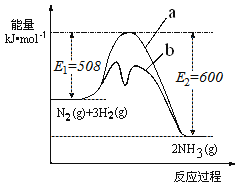
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是_____________。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n molN2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)500℃、50MPa时,在容积为1 L的容器中加入1 mol N2、3 mol H2,反应达平衡后测得平衡常数为K,此时N2的转化率为a。则K和a的关系是K=_______________。
(4)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) |
ⅰ | 450 |
| 1 |
ⅱ | ______ |
| 10 |
ⅲ | 480 | ______ | 10 |
(5)1998年希腊亚里斯多德大学的两位科学家采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电解合成氨。其实验装置如图。阴极的电极反应式为________________________。
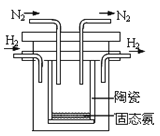
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期中的四种主族元素A、B、C、D、E,原子序数依次增大。A是电负性最大的元素,B、D的价电子层中均有两个未成对电子,回答下列问题:
(1)B元素在周期表中的位置为___________________________;
(2)A的基态原子中,电子占据的最高能级符号为___;该能级的电子云轮廓图形状为__________;
(3)B、C、D三种元素的第一电离能大小顺序为________;该电离能大小变化的原因为________________;
(4)C、D、E三种元素的最高价氧化物的水化物的酸性强弱顺为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因是:________。
(2)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下:
①CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H=+210.5kJ· mol-1
②CaSO4(s)+4CO(g) CaS(s)+ 4CO2(g) △H=-189.2 kJ· mol-1
反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g) △H=____kJ· mol-1
(3)在恒温条件下,1 mol NO2和足量C发生反应2NO2(g)+2C(s)![]() N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
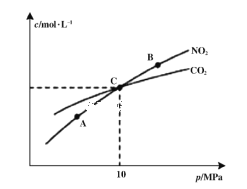
①A、B两点的浓度平衡常数关系:Kc(A) ____Kc(B)(填“<”或“>”或“=”)
②A、B、C三点中NO2的转化率最高的是____(填“A”或“B”或“C”)点。
(4)已知:亚硝酸(HNO2)性质和硝酸类似,但它是一种弱酸。常温下亚硝酸的电离平衡常数Ka=5.1×10-4;H2CO3的Ka1=4.2×10-7,Ka2=5.61×10-11。在常温下向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小的顺序是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶。制备它的一种配方中含有下列四种物质:
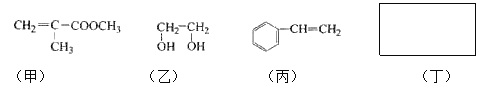
填写下列空白:
(1)甲中不含氧原子的官能团是____________;下列试剂能与甲反应而褪色的是___________(填标号)
a. Br2/CCl4溶液 b.石蕊溶液 c.酸性KMnO4溶液
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:_______
(3)淀粉通过下列转化可以得到乙(其中A—D均为有机物):

A的分子式是___________,试剂X可以是___________。
(4)已知: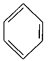 +RCl
+RCl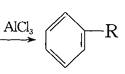 +HCl(-R为烃基)
+HCl(-R为烃基)
 +H2
+H2
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是 ______________ 。
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110。丁与FeCl3溶液作用现特征颜色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸合成治疗禽流感的药物—达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
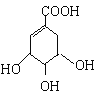
(提示:环丁烷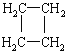 可简写成
可简写成![]() )
)
(1)A的分子式是_______
(2)A与溴的四氯化碳溶液反应的化学方程式(有机物用结构简式表示)_____
(3)A与乙醇反应的化学方程式(有机物用结构简式表示)是_______
(4)17.4g A与足量碳酸氢钠溶液反应,计算生成二氧化碳的体积(标准状况)____L
(5)A在浓硫酸作用下加热可得到B(B的结构简式为![]() ),其反应类型是____。
),其反应类型是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠晶体(Na2MoO4.2H2O)是一种无公害型冷却水系统的金属缓蚀剂。工业上利用钼精矿(主要成分是不溶于水的MoS2)制备钼酸钠的两种途径如图所示:
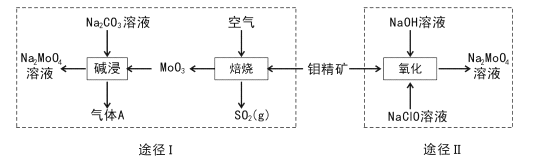
(l) Na2 MoO4![]() 2H2O中钼元素的化合价为____,NaCIO的电子式为 ___。
2H2O中钼元素的化合价为____,NaCIO的电子式为 ___。
(2)途径I为了提高钼精矿焙烧速率,可采取的措施是____(答出两条即可)。
(3)途径I焙烧过程中化学方程式为____,碱浸时气体A的化学式为____。
(4)已知途径I的钼酸钠溶液中c(MoO42-)=0. 40mol/L,c(CO32-)=0. 20mol/L。由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去CO32-。当BaMoO4开始沉淀时,CO32-的去除率是____(已知Ksp(BaCO3) =1×10-9、Ksp(BaMo04) =4.0×10-8,忽略溶液的体积变化)。
(5)途径II氧化时溶液中还有Na2SO4生成,则还原剂与氧化剂物质的量之比为_____。
(6)途径I或途径II所得的Na2MoO4溶液经结晶可得固体A后再重结晶可得固体B,其重结晶操作的目的为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com