
| A. | 反应①中试剂X是氢氧化钠溶液 | |
| B. | 试剂Y是HCI,它与AlO2-反应生成氢氧化铝 | |
| C. | 图中所示转化反应中包含2个氧化还原反应 | |
| D. | 将X与Y试剂进行对换,最终可以达到相同结果 |
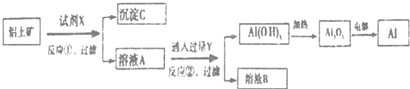
分析 综合分析工艺流程图可知,试剂X是氢氧化钠溶液,Al2O3溶于氢氧化钠溶液得到NaAlO2溶液,Fe2O3与氢氧化钠溶液不反应,所以反应①过滤后所得溶液A为NaAlO2溶液,沉淀C为Fe2O3;Y为CO2,向NaAlO2溶液中通入过量CO2的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,溶液B为NaHCO3,电解熔融Al2O3属于氧化还原反应,以此解答该题.
解答 解:A.分离氧化铝和氧化铁,只能用氢氧化钠溶液,不可能用盐酸,因氧化铝与氢氧化钠反应,氧化铁不反应,但二者都可与盐酸反应,故A正确;
B.如试剂Y是HCl,过量HCl与AlO2-反应生成氯化铝,不可能得到氢氧化铝,故B错误;
C.只有电解熔融Al2O3属于氧化还原反应,故C错误;
D.因二氧化碳与氧化铁、氧化铝都不反应,则将X与Y试剂进行对换,不能对物质进行分离,故D错误;
故选A.
点评 本题以铁、铝化合物的性质为载体综合考查工业冶炼铝等知识,侧重于考查学生分析和解决问题的能力,综合性强,为高考常见题型,注意把握制备原理和反应的流程,难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑥ | B. | ①②④⑤⑥ | C. | ②③④⑤⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水银、硫酸、烧碱、硫酸氢钠 | B. | 氯水、盐酸、火碱、硫酸钡 | ||
| C. | 臭氧、硝酸、纯碱、胆矾 | D. | 铜、醋酸、石灰石、氯化铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HX,HZ,HY | B. | HX,HY,HZ | C. | HZ,HY,HX | D. | HY,HZ,HX |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的干馏、石油的分馏分别是化学变化、物理变化 | |
| B. | 用饱和碳酸钠溶液除去乙酸乙酯中少量的乙酸 | |
| C. | 可以用新制的氢氧化铜检验尿液中的葡萄糖 | |
| D. | 在蛋白质溶液中滴加饱和硫酸铵溶液可以使蛋白质变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 d.CH2=CHCH3.
d.CH2=CHCH3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com