
化学卷·2015届浙江省嘉兴市高三上学期学科基础测试(201409)】30.(本题10分)实验室从含碘废液(除H2O外,含有CCl4, I2, I-等)中回收碘,其实验过程如下:

(1)操作x的名称为________________。主要的仪器是_______________________。
(2)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的 I2 还原为I-,其离子方程式为_________;该操作的目的是____________________。
(3)①在测定亚硫酸钠溶液浓度时,量取25.00mL亚硫酸钠溶液,用0.10mol·L-1的酸性高锰酸钾溶液进行滴定,下列说法正确的是_________________。
A.润洗滴定管时,应从滴定管上口加满所需的试液,使滴定管内壁充分润洗
B.高锰酸钾溶液装在酸式滴定管中,本实验无需外加指示剂
C.滴定时,眼睛注视滴定管中液面的变化
D.滴定开始时读数正确,滴定终点仰视读数,会使实验误差偏高
②达到滴定终点时,消耗高锰酸钾溶液18.00mL,则亚硫酸钠溶液的浓度为________________。
【知识点】氧化还原反应、离子反应方程式,滴定操作B2 B1
【答案解析】(1) 分液 (1分) 分液漏斗(答出分液漏斗就得分) (1分)
(2)SO32-+I2+H2O=2I-+SO42-+2H+ (2分) 使四氯化碳当中的碘单质进入水溶液中(2分)
(3)①B、D(2分,漏答给1分,错答不给分) ②c(Na2SO3)==0.18 mol·L-1(2分)
解析:(1)四氯化碳属于有机物、水属于无机物,二者不互溶,分离互不相溶的液体采用分液的方法分离,所以分离出四氯化碳采用分液的方法,使用的仪器是分液漏斗;
(2)碘具有氧化性,能氧化亚硫酸钠生成硫酸钠,自身被还原生成碘,离子反应方程式为SO32-+I2+H2O=2I-+2H++SO42-;由于碘不容易溶于水,但碘离子易溶于水,为了使更多的I元素进入水溶液应将碘还原为碘离子;
(3)①A.润洗滴定管时,不需要加满所需的试液,故错误;
B.高锰酸钾溶液有强氧化性,能氧化橡胶管,所以高锰酸钾溶液装在酸式滴定管中,由于反应过程中溶液的颜色会发生变化,本实验无需外加指示剂,故正确;
C.滴定时,眼睛注视锥形瓶中溶液颜色的变化,故错误;
D.滴定开始时读数正确,滴定终点仰视读数,导致读取的高锰酸钾溶液体积偏大,会使实验误差偏高,故正确;
②根据电子守恒,得到关系式:
5Na2SO3----- 2KMnO4
5 2
0.025c 0.1×0.018
解得:c=0.18 (mol·L-1)
【思路点拨】本题以物质的制备为载体考查了氧化还原反应、离子反应方程式,滴定操作等,最后的计算根据电子守恒,得到关系式:5Na2SO3----- 2KMnO4是关键。


科目:高中化学 来源: 题型:
向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
(1)写出反应的离子方程式___________________________
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号).
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
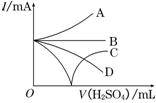
(3)若缓缓加入稀H2SO4直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用右图中的曲线表示是________(填序号).
(4)若向装有Ba(OH)2溶液烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应.则反应的离子方程式是 _________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
二草酸合铜(Ⅱ)酸钾晶体{K2[Cu(C2O4)2]·2H2O}制备流程如下:
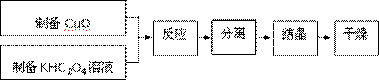
(1)制备CuO:CuSO4溶液中滴入NaOH溶液,加热煮沸、冷却、双层滤纸过滤、洗涤。
①过滤所需的玻璃仪器有
②用蒸馏水洗涤氧化铜时,如何证明氧化铜已洗涤干净
(2)①为提高CuO的利用率,让滤纸上的CuO充分转移到热的KHC2O4溶液中,以下方案正确的是
a.剪碎滤纸,加入到热的KHC2O4溶液中,待充分反应后趁热过滤
b.用稀硫酸溶解滤纸上的氧化铜,然后将溶液转入热的KHC2O4溶液中
c.用氢氧化钾溶液溶解氧化铜,并转入热的KHC2O4溶液中
d.在空气中灼烧滤纸,将剩余的固体转入热的KHC2O4溶液
②50℃水浴加热至反应充分,发生反应的化学方程式为 ;再经趁热过滤、沸水洗涤、将滤液蒸发浓缩得到二草酸合铜(Ⅱ)酸钾晶体。
(3)本实验用K2CO3粉末与草酸溶液反应制备KHC2O4,此反应进行的主要原因是 。
(4)二草酸合铜(Ⅱ)酸钾晶体的制备也可以用CuSO4晶体和K2C2O4溶液反应得到。从硫酸铜溶液中获得硫酸铜晶体的实验步骤为:加入适量乙醇、蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
①加入适量乙醇的优点有:
a.缩短加热的时间,降低能耗; b. 。
②在蒸发浓缩的初始阶段还采用了蒸馏的操作,其目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
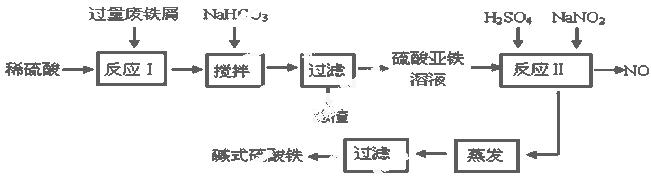
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)加入少量NaHCO3的目的是调节pH在 范围内,使溶液中的 沉淀(写离子符号)。
(2)反应Ⅱ中加入NaNO2的目的是 发生反应的离子方程式为
(3)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2有11.2 L(标准状况),则相当于节约NaNO2的物质的量为 。
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,Fe(OH)2+可部分水解生成Fe2(OH)42+ 聚合离子,该水解反应的离子方程式为
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的最佳试剂为 。
A.溴水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中所示物质或概念间的从属关系符合右图的是
| X | Y | Z | |
| A. | 钠元素 | 主族元素 | 短周期元素 |
| B. | 电解质 | 化合物 | 纯净物 |
| C. | 氢氧化铁 | 胶体 | 分散系 |
| D. | 置换反应 | 氧化还原反应 | 放热反应 |

查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用NaNO2+NH4Cl=NaCl+N2↑+2H2O制备N2,下列说法正确的是( )
A.NaNO2发生氧化反应
B.NH4Cl中的氮元素被还原
C.N2既是氧化产物,又是还原产物
D.每生成1mol N2转移电子的物质的量为6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
有关蛋白质的叙述正确的是 ( )
A.蛋白质溶液中,加入浓的硫酸铵溶液有沉淀析出,加水后沉淀不溶解
B.蛋白质属于天然高分子化合物
C.蛋白质的分子能透过半透膜
D.蛋白质跟浓盐酸作用时呈黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质中既具有相同的最简式,又不属于同分异构体和 同系物的是 ( )
同系物的是 ( )
①聚乙烯和乙烯 ②甲醛和葡萄糖 ③淀粉和纤维素
④蔗糖和麦芽糖 ⑤聚乙烯和聚氯乙烯
A.①②⑤ B.①②③
C.①③⑤ D.①②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
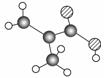
某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。
(1)该物质的结构简式为
________________________________________________________________________。
(2)该物质中所含官能团的名称为________________________。
(3)下列物质中,与该产品互为同系物的是(填序号)________,互为同分异构体的是__________。
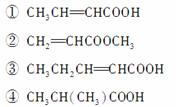
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com