
| A. | 推广使用一次性木筷,减少疾病传染 | |
| B. | 将地沟油回收重新加工为食用油,提高资源的利用率 | |
| C. | 推广使用电动汽车、天然气汽车等公共交通工具,保护环境 | |
| D. | 推广使用煤的气化、液化技术可减少二氧化碳等温室气体的排放 |
分析 A.使用一次性木筷,浪费大量的木材;
B.地沟油含致癌性物质;
C.使用电动汽车、天然气汽车等公共交通工具,减少化石能源的使用,减少尾气的排放;
D.煤的气化、液化不能减少二氧化碳的排放.
解答 解:A.使用一次性木筷,浪费大量的木材,不符合可持续发展的要求,故A不选;
B.地沟油含致癌性物质,不能回收重新加工为食用油,影响人类健康,故B不选;
C.使用电动汽车、天然气汽车等公共交通工具,减少化石能源的使用,减少尾气的排放,则可保护环境,故C选;
D.煤的气化、液化不能减少二氧化碳的排放,不能控制温室效应,故D不选;
故选C.
点评 本题考查三废处理及环境保护,为高频考点,把握化学与生活、环境、能源的联系为解答的关键,侧重分析与应用能力的考查,注意可持续发展的意义,题目难度不大.


 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | K+、H+、NO3 -、HCO3- | B. | Na+、K+、SO42-、ClO- | ||
| C. | K+、Al 3+、OH-、Cl- | D. | Fe2+、H+、Cu 2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 在上述条件下,SO2不可能100%地转化为SO3 | |
| C. | 为了提高SO2的转化率,应适当提高O2的浓度 | |
| D. | 达到平衡时,SO2的浓度与SO3的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,有关它的说法正确的是( )
,有关它的说法正确的是( )| A. | 它属于芳香烃 | B. | 分子中最多有25个原子共面 | ||
| C. | 分子式为C14H8Cl5 | D. | 1 mol该物质能与6 molH2加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 | |
| B. | 乙酸与乙醇可发生酯化反应,均可与金属钠发生置换反应 | |
| C. | 分馏、干馏都是物理变化,裂化、裂解都是化学变化 | |
| D. | 石油经过分馏得到多种烃,煤经过分馏可制焦炭、煤焦油等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高NH4Cl溶液的温度,其水的离子积常数和pH均增大 | |
| B. | 在有AgI沉淀的上层清液中滴加一定浓度的NaCl溶液,不可能产生白色沉淀 | |
| C. | pH=3的盐酸与pH=11的氨水等体积混合后,溶液中:c(NH4+>c(Cl-)>c(OH-)>c(H+) | |
| D. | 室温下,稀释0.1mol•L-1CH3COOH溶液,溶液的导电能力增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CuSO4和Cu(NO3)2是自然界中重要的铜盐.请回答下列问题:
CuSO4和Cu(NO3)2是自然界中重要的铜盐.请回答下列问题: (用箭头表示出配位键的位置)
(用箭头表示出配位键的位置)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1的HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) | |
| B. | 等浓度、等体积的Na2CO3和NaHCO3混合:$\frac{c(HC{O}_{3}^{-})}{c({H}_{2}C{O}_{3})}$>$\frac{c(C{O}_{3}^{2-})}{c(HC{O}_{3}^{-})}$ | |
| C. | 0.1 mol•L-1的NaHCO3溶液中:c(Na+)+c(H+)=c(HCO${\;}_{3}^{-}$)+2c(CO${\;}_{3}^{2-}$)+c(OH-) | |
| D. | 等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 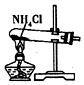 制取氧气 | B. | 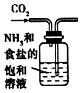 制取NaHCO | C. | 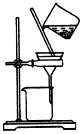 分离NaHCO3 | D. | 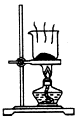 干燥NaHCO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com