
| A. | O2+4H++4e-=2H2O | B. | O2+2H2O+4e-=4OH- | ||
| C. | N2H4+4OH--4e-=N2+4H2O | D. | N2H4+4H++2e-=2NH4+ |
分析 4NH3+3O2═2N2+6H2O设计成原电池,所以氨气是负极,发生氧化反应,而氧气是正极反应还原反应,由此分析解答.
解答 解:A、在酸介质中正极发生电极反应式为:O2+4H++4e-=2H2O,故A正确;
B、在碱性介质中,正极的电极反应式为:O2+2H2O+4e-=4OH-,故B正确;
C、碱性介质中,负极的电极反应式为:2NH3+6OH--6e-=N2+6H2O,故C错误;
D、在酸性介质中电极反应式为:2NH3-6e-=N2+6H+,故D 错误;
故选CD.
点评 本题考查电极反应式的书写,为高频考点,明确各个电极上发生的反应是解本题关键,电极反应式的书写也是学习难点,注意结合电解质溶液酸碱性书写,题目难度中等.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2?Ba2++2 OH- | B. | H3PO4?3 H++PO43- | ||
| C. | NaHCO3═Na++H++CO3 2- | D. | HClO?H++ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HC1的电子式: | B. | 乙烯分子的结构简式:CH2CH2 | ||
| C. | S2-的原子结构示意图: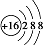 | D. | H2O2的电子式: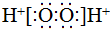 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 弱电解质 | H2CO3 | NH3•H2O |
| 电离平衡常数 | Ka1=4.30×10-7 Ka2=5.61×10-11 | 1.77×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
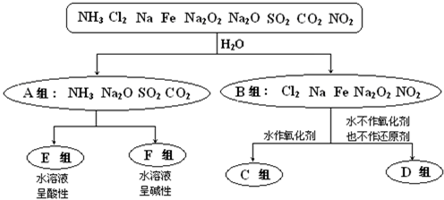
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com