
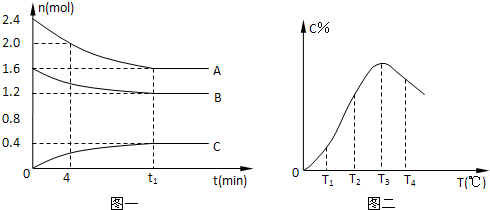
| A、0~4分钟时,A的平均反应速率为0.02mol/(L?min) | ||
B、该反应的平衡常数表达式K=
| ||
| C、由T1向T2变化时,V正>V逆 | ||
| D、此反应的正反应为吸热反应 |
| △c |
| △t |
| ||
| △t |
| ||
| 4min |
| c(C) |
| c2(A)?c(B) |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、先加HCl,再加HBr |
| B、先加Cl2再加HBr |
| C、先加HCl,再加Br2 |
| D、先加HBr,再加HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④ | B、①②③ |
| C、①②④ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡是核电荷数相同的原子,一定属于同一种元素 |
| B、不同种元素的原子,质量数必定不同,同种元素的原子,质量数必定相同 |
| C、凡是核电荷数相同的微粒,一定属于同一种元素 |
| D、人们已经知道了108种元素,所以人们已经知道了108种原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用连有小灯泡的电路测硫酸溶液的导电性,灯泡较亮 |
| B、能跟锌反应产生氢气 |
| C、1mol/L硫酸溶液中H+浓度为2mol/L |
| D、能与碳酸钠反应放出二氧化碳气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( )| A、在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX | ||
| B、根据滴定曲线,可得Ka(HY)≈10-5 | ||
| C、将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+) | ||
D、HY与HZ混合,达到平衡时:c(H+)=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1个金属原子失去电子的多少 |
| B、1mol金属与酸反应放出氢气的多少 |
| C、1mol金属失去电子的多少 |
| D、金属原子失去电子的难易程度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com