
某探究小组利用丙酮的溴代反应(CH3COCH3+B r2
r2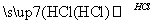 CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:
| 实验 | 初始浓度c/mol/L | 溴颜色消失所需时间t/s | ||
| 序号 | CH3COCH3 | HCl | Br2 | |
| ① ② ③ ④ | 0.80 1.60
0.80 | 0.20 0.20 0.40 0.20 | 0.0010 0.0010 0.0010 0.0020 | 290 145
580 |
分析实验数据所得出的结论不正确的是 ( )
A.增大c(CH3COCH3),v(Br2)增大
B.实验②和③的v(Br2)相等
C.增大c(HCl),v(Br2)增大
D.增大c(Br2),v(Br2)增大
科目:高中化学 来源: 题型:
ClO2是饮用水消毒剂.用ClO2处理过的饮用水(pH为5.5~6.5)除含有ClO2外,常含有一定量对人体不利的ClO2﹣.为测定此饮用水中两者成分,进行如下实验:准确量取v mL水样加入到锥形瓶中,调节水样pH=8,加人足量KI晶体,发生如下反应:2ClO2+2I﹣=I2+2ClO2﹣,反应结束后产生amol I2;继续调节溶液pH=1,又发生如下反应:ClO2﹣+4H+=2I2+Cl﹣+2H2O,反应结束后叉产生b mol I2.饮用水中c(ClO2﹣)= 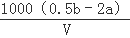 mol•L﹣ 1(用含字母的代数式表示).
mol•L﹣ 1(用含字母的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿[主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等]制取CoCl2·6H2O的工艺流程如下:
 |
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式 。
 (2)NaClO3的作用是 。
(2)NaClO3的作用是 。
(3)加Na2CO3调pH至5.2所得沉淀为
。
(4)萃取剂对金属离子的萃取率与pH的关系如图。
萃取剂的作用是 ;
其使用的较适宜pH范围是 。
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
(5)为测定粗产品中CoCl2·6H2O含量,称取一定质
量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是
。(答一条即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
将1L 0.1 mol·L-1 BaCl2溶液与足量稀硫酸充分反应放出a kJ热量;将1L 0.5 mol·L-1 HCl溶液与足量CH3COONa溶液充分反应放出b kJ热量(不考虑醋酸钠水解);将0.5L 1 mol·L-1 H2SO4溶液与足量(CH3COO)2Ba(可溶性强电解质)溶液反应放出的热量为( )
A.(5a+2b) kJ B.(4b-10a) kJ C.(5a-2b) kJ D.(10a+4b) kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
硫—碘循环分解水制氢主要涉及下列反应 :
:
Ⅰ SO2+2H2O+I2===H2SO4+2HI
Ⅱ 2HI H2+I2
Ⅲ 2H2SO4===2SO2+O2+2H2O
(1)分析上述反应,下列判断正确的是________。
a.反应Ⅲ易在常温下进行
b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O
d.循环过程产生1 mol O2的同时产生1 mol H2
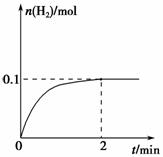 (2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示。
(2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示。
0~2 min内的平均反应速率
v(HI)=________。该温度下,
H2(g)+I2(g) 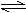 2HI(g)的平衡常数K=________。
2HI(g)的平衡常数K=________。
相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则________是原来的2倍。
a.平衡常数 b.HI的平衡浓度
c.达到平衡的时间 d.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡________移动(填“向左”、“向右”或“不”);若加入少量下列试剂中的________,产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(4)以H2为燃料可制作氢氧燃料电池。
已知2H2(g)+O2(g)===2H2O(l) ΔH=-572 kJ·mol-1某氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,该电池的能量转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)实验室配制好的硅酸钠溶液保存过程中变质的主要原因是________________________________________________________________________,
变质现象是________,相应化学方程式是______________________________。
(2)盛放烧碱等碱性溶液不宜用磨口玻璃塞。因为__________________________ ____________________________________________________________________________,
写出相应的离子方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸在反应中的价态变化:向铜片中加入浓硝酸,回答下列问题:
(1)开始阶段实验现象为:____________________ ______________。
反应的化学方程式为:__________________________________。
(2)若铜有剩余,则临近结束时的反应方程式为:________________________________________________________________________。
(3)当反应结束后,若通过分液漏斗向烧瓶内再加入稀盐酸,又可继续反应,产生无色无味的气体,此时的离子方程式可表示为:________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com