
(1)含碳物质不完全燃烧会产生CO。血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒,写出铁离子(Fe3+)的核外电子排布式为 ,CO有多种等电子体,其中常见的一种分子是 。利用CO可以合成化工原料COCl2、配合物Fe(CO)5等,已知一个COCl2分子中每个原子最外层都形成8电子的稳定结构,则一个COCl2分子内含有 个δ键,C原子的杂化方式为 。Fe(CO)5等在一定条件下分解生成CO和铁,反应过程中断裂的化学键是 ,形成的化学键是 。
(2)A、B均为短周期金属元素。依据下表数据,回答问题:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
写出A原子的电子排布图 ,Al原子的第一电离能 (填:“大于”、“小于”或“等于”)738 kJ·mol-1,原因是 。
(3)下图是一种镍(Ni)镧(La)合金储氢后的晶胞结构图。该合金储氢后,含0.5mol Ni的合金可吸附氢气的体积(标况)为 。

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
硫酸亚铁(FeSO4·7H2O)是一种重要的食品和饲料添加剂。实验室通过如下实验由废铁屑制备
FeSO4·7H2O晶体:
① 将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2至3遍;
② 向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50-80℃之间至铁屑耗尽;
③ 趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④ 待结晶完毕后,滤出晶体,用少量冰水洗涤2-3次,再用滤纸将晶体吸干;
⑤ 将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。
请回答下列问题:
⑴ 实验步骤①的目的是____________________,加热的作用是__________________。
⑵ 实验步骤②明显不合理,理由是_______________________________。
⑶ 实验步骤④中用少量冰水洗涤晶体,其目的是______________;______________。
⑷ 经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4·7H2O、FeSO4·4H2O、和FeSO4·H2O。硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示(仅在56.7℃、64℃温度下可同时析出两种晶体)。
硫酸亚铁的溶解度和析出晶体的组成
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 | ||
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27 | ||
| 析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | |||||||||
请根据表中数据作出硫酸亚铁的溶解度曲线。

⑸ 若需从硫酸亚铁溶液中结晶出FeSO4·4H2O,应控制的结晶温度(t)的范围为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性
②取少量溶液中入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体
③在上述溶液中再滴加Ba(NO3)3溶液,产生白色沉淀
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀
根据实验以下推测正确的是 ( )
A.一定有SO32-离子 B.一定有CO32-离子
C.Cl-离子一定存在 D.不能确定HCO 离子是否存在
离子是否存在
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应mA(g)+nB(s) rC(g)+qD(g)在反应过程中,其他条件不变,D的体积百分 含量和温度T 或压强P关系如图所示,下列叙述中正确的是( )
rC(g)+qD(g)在反应过程中,其他条件不变,D的体积百分 含量和温度T 或压强P关系如图所示,下列叙述中正确的是( )

A.化学方程式系数m+n = r+q
B.使用催化剂,D的物质的量分数增加
C.温度降低,化学平衡向正反应方向移动
D.物质B的颗粒越小,反应越快,有利于平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8960 mL的NO2气体和672 mLN2O4的气体(都已折算到标准状态),在反应后的溶液中加足量的氢氧化钠溶液,生成沉淀质量为17.02g。则x等于 ( )
A.8.64g B.9.44g C.9.00g D. 9.20g
查看答案和解析>>
科目:高中化学 来源: 题型:
向盛有50mL 1.00 mol·L-1HCl溶液的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如右图所示,下列不正确的是( )
A.该实验表明化学能可以转化为热能
B.NaOH溶液的浓度大于1.00 mol·L-1
C.V=50mL时,混合液的pH>7
D.该实验表明有水生成的反应都是放热反应

查看答案和解析>>
科目:高中化学 来源: 题型:
氯原子对O3分解有催化作用:
O3 + Cl =ClO + O2 ΔH1 ClO + O =Cl + O2 ΔH2
大气臭氧层的分解反应是:O3 + O=2O2 ΔH,该反应的能量变化如图:
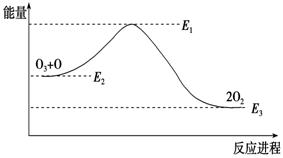
下列叙述中,正确的是( )
A.反应O3 + O =2O2的ΔH=E1-E3 B.O3 + O =2O2是吸热反应
C.ΔH=ΔH1+ΔH2 D.大气层中的臭氧无法再生
查看答案和解析>>
科目:高中化学 来源: 题型:
最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的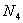 分子。
分子。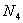 分子结构如右图所示,已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ。根据以上信息和数据,下列说法正确的是
分子结构如右图所示,已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ。根据以上信息和数据,下列说法正确的是
A.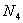 属于一种新型的化合物
属于一种新型的化合物
B.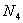 与
与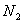 互为同素异形体
互为同素异形体
C.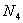 沸点比
沸点比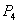 (白磷)高
(白磷)高
D.1mo1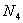 气体转变为
气体转变为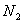 将吸收882kJ热量
将吸收882kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
从H、O、C、Ca四种元素中,选择适当的元素组成符合下列要求的一种物质,并
用化学式填空。
(1)具有可燃性,可做火箭燃料的是 。
(2) 相对分子质量最小的氧化物是 。
相对分子质量最小的氧化物是 。
(3)大理石或石灰石的主要成分都是  。
。
(4)可做温室肥料,固体可用于人工降雨的是 。
(5)农业上可供用来改良酸性土壤的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com