
ЁОЬтФПЁПЃЈЬтЮФЃЉЂёЃЎЛЏбЇПЮЩЯРЯЪІбнЪОСЫШчЯТЭМЕФЪЕбщЃК
ЪЕбщЪБЃЌНЋСНЦјЧђФкЕФNaHCO3КЭNa2CO3ЭЌЪБЕЙШыЪдЙмжаЁЃвбжЊбЮЫсЪЧзуСПЕФЃЌЧвећЬззАжУЦјУмадСМКУЃЌЛиД№ЯТСаЮЪЬтЃК
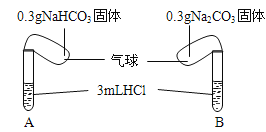
ЃЈ1ЃЉЪЕбщЙ§ГЬжаЙлВьЕНЕФЯжЯѓЪЧЃК________________ЃЎ
ЃЈ2ЃЉЪЕбщНсЪјКѓЃЌСНЪдЙмЕФЦјЧђДѓаЁгаВювьЃЌДѓаЁЦјЧђЃЈАќКЌЪдЙмЃЉЬхЛ§жЎБШдМЮЊЃЈЬюзюМђЕЅећЪ§БШЃЉ__________ЃЎ
ЂђЃЎЕБМзЭЌбЇгУЪжДЅУўЩЯЪіЪдЙмЪБЃЌвтЭтЗЂЯжAЪдЙмБфРфЃЌЖјBЪдЙмЗЂШШЃЌЫћАбетИіЗЂЯжИцЫпСЫЭЌзРввЭЌбЇЃЌВЂгЩДЫЕУГіНсТлЃКNaHCO3КЭHClЗДгІЮЊЮќШШЗДгІЃЌЖјNa2CO3КЭHClЗДгІЮЊЗХШШЗДгІЃЎввЭЌбЇШДЖдДЫНсТлШДГжЛГвЩЕФЬЌЖШЃЎЮЊДЫЃЌСНЮЛЭЌбЇдкПЮЭтЛюЖЏжаМЬајНјааСЫЯТСаЪЕбщЃЈУПДЮЪЕбщИїзі3ДЮЦНааЪЕбщЃЌШЁЦНОљжЕЃЉЃК
ађКХ | ЪдМС1 | ЪдМС2 | ЛьКЯЧАЮТЖШ | ЛьКЯКѓЮТЖШ |
Ђй | 35mLЫЎ | 2.5g NaHCO3ЙЬЬх | 20Ёц | 18.5Ёц |
Ђк | 35mLЫЎ | 3.2g Na2CO3ЙЬЬх | 20Ёц | 24.3Ёц |
Ђл | 35mLЯЁбЮЫс | КЌ2.5g NaHCO3ЕФБЅКЭШмвК32.5mL | 20Ёц | 19Ёц |
Ђм | 35mLЯЁбЮЫс | КЌ3.2g Na2CO3ЕФБЅКЭШмвК23.1mL+10mLЫЎ | 20Ёц | 24.2Ёц |
Ђн | 35mLЯЁбЮЫс | 2.5g NaHCO3ЙЬЬх | 20Ёц | 16.2Ёц |
Ђо | 35mLЯЁбЮЫс | 3.2g Na2CO3ЙЬЬх | 20Ёц | 25.1Ёц |
ЧыФуАяжњЬюаДЯрЙиФкШнЃК
ЃЈ1ЃЉИУбаОПБЈИцЕФЬтФПЪЧЁЖ___________________________ЁЗЃЎ
ЃЈ2ЃЉИУЪЕбщжаЫљгУЕФвЧЦїГ§ЪдЙмЁЂвЉГзЃЈЛђVаЭжНВлЃЉЁЂЦјЧђЁЂВЃСЇАєЁЂЩеБЁЂСПЭВЁЂБЃЮТЦПЭтЃЌЛЙашвЊЕФвЧЦїУћГЦЪЧ______________________ЃЎ
ЃЈ3ЃЉЪЕбщЂйКЭЂкЕФФПЕФЪЧ_________________________________________________ЃЎ
ЃЈ4ЃЉЭЈЙ§ЩЯЪіЪЕбщПЩЕУГіЕФНсТлЪЧЃК___________________________________ЃЈаДГіСНЬѕМДПЩЃЉЃЎ
ЁОД№АИЁПСНжЇЪдЙмжаЖМВњЩњДѓСПЦјХнЃЌЦјЧђХђеЭЃЌAЪдЙмжаВњЩњЦјЬхЕФЗДгІЫйТЪвЊПьЕУЖр53ЃК42NaHCO3ЁЂNa2CO3КЭбЮЫсЗДгІЙ§ГЬжаШШаЇгІЕФбаОПЮТЖШМЦЁЂЬьЦНбаОПNaHCO3ЙЬЬхЁЂNa2CO3ЙЬЬхгыбЮЫсЗДгІЪБЮТЖШЕФБфЛЏЪЧЗёЪЧгЩгкЙЬЬхШмгкЫЎв§Ц№ЕФNaHCO3ЙЬЬхгыбЮЫсЗДгІЪБЃЌЮТЖШНЕЕЭЃЌдвђЪЧNaHCO3ЙЬЬхШмгкЫЎЪБЮќШШЃЌNaHCO3гыбЮЫсЕФЗДгІвВЪЧЮќШШЗДгІЃЛNa2CO3ЙЬЬхгыбЮЫсЗДгІЪБЃЌЮТЖШЩ§ИпЃЌдвђЪЧNa2CO3ЙЬЬхШмгкЫЎЪБЗХШШЃЌNa2CO3гыбЮЫсЕФЗДгІвВЪЧЗХШШЗДгІ
ЁОНтЮіЁП
ЂёЃЎЃЈ1ЃЉвђЮЊЁАбЮЫсЪзЯШгыЬМЫсФЦЗДгІЩњГЩЬМЫсЧтФЦЃЌУЛгаЖўбѕЛЏЬМВњЩњЃЌШЛКѓгыЬМЫсЧтФЦЗДгІЃЌЩњГЩЖўбѕЛЏЬМЁБЃЌЫљвдЃЌзАгаNaHCO3ШмвКЕФЪдЙмжаКмПьВњЩњЦјХнЃЌЖјзАгаNa2CO3ШмвКЕФЪдЙмжаПЊЪМУЛгаЦјХнВњЩњЃЌЕЋЫцзХЕЮШыЯЁбЮЫсЕФСПдіМгЃЌВХЛсВњЩњЦјХнЃЌЙЪД№АИЮЊЃКСНжЇЪдЙмжаЖМВњЩњДѓСПЦјХнЃЌЦјЧђХђеЭЃЌAЪдЙмжаВњЩњЦјЬхЕФЗДгІЫйТЪвЊПьЕУЖрЃЛ
ЃЈ2ЃЉбЮЫсгыЬМЫсФЦЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃКNa2CO3+HCl=NaCl+NaHCO3ЃЌбЮЫсгыЬМЫсЧтФЦЗДгІЕФЛЏбЇЗНГЬЮЊЃКNaHCO3+HCl=NaCl+H2O+CO2ЁќЃЌИљОнЖўепгыбЮЫсЗДгІЕФЛЏбЇЗНГЬЪНПЩжЊЃЌNa2CO3ЕФЯрЖдЗжзгжЪСПБШЕФДѓNaHCO3ЕФДѓЃЌЙЪЯрЭЌжЪСПЕФNa2CO3гыNaHCO3жаЃЌNaHCO3КЌгаЕФЗжзгЖрвЛаЉЃЌМДNaHCO3гыбЮЫсЗДгІЩњГЩЕФCO2ЦјЬхЖрвЛаЉЃЌЫљвдAЪдЙмЕФЦјЧђДѓЃЌ
NaHCO3 ЁЋЁЋЁЋЁЋCO2ЃЌ
1mol 1mol
![]()
![]() ЃЌ
ЃЌ
Na2CO3 ЁЋЁЋЁЋЁЋCO2ЃЌ
1mol 1mol
![]()
![]()
дђ0.3gNaHCO3ЛђNa2CO3ЗлФЉгызуСПбЮЫсЗЂЩњЗДгІВњЩњЕФЦјЬхЬхЛ§жЎБШЮЊЃК![]() ЃК
ЃК![]() =53ЃК42ЃЌЙЪД№АИЮЊЃК53ЃК42ЃЛ
=53ЃК42ЃЌЙЪД№АИЮЊЃК53ЃК42ЃЛ
ЃЈ1ЃЉИљОнБОЪЕбщЕФЪ§ОнгыЪЕбщНсТлжЊЃЌИУЪЕбщЕФПЮЬтЪЧЁЖNaHCO3ЁЂNa2CO3КЭбЮЫсЗДгІЙ§ГЬжаШШаЇгІЕФбаОПЁЗЃЛЙЪД№АИЮЊЃКNaHCO3ЁЂNa2CO3КЭбЮЫсЗДгІЙ§ГЬжаШШаЇгІЕФбаОПЃЛ
ЃЈ2ЃЉгЩЭМБэжЊЃЌИУЪЕбщжаШБЩйВтСПЮТЖШЕФвЧЦї-ЮТЖШМЦКЭВтСПЙЬЬхжЪСПЕФвЧЦї-ЬьЦНЃЌЙЪД№АИЮЊЃКЮТЖШМЦЃЛЬьЦНЃЛ
ЃЈ3ЃЉЪЕбщЂйКЭЂкЗжБ№ЮЊЬМЫсЧтФЦЁЂЬМЫсФЦЙЬЬхШмгкЫЎЕФШШаЇгІЃЌЦфФПЕФЪЧбаОПNaHCO3ЙЬЬхЁЂNa2CO3ЙЬЬхгыбЮЫсЗДгІЪБЮТЖШЕФБфЛЏЪЧЗёЪЧгЩгкЙЬЬхШмгкЫЎв§Ц№ЕФЃЌЙЪД№АИЮЊЃКбаОПNaHCO3ЙЬЬхЁЂNa2CO3ЙЬЬхгыбЮЫсЗДгІЪБЮТЖШЕФБфЛЏЪЧЗёЪЧгЩгкЙЬЬхШмгкЫЎв§Ц№ЕФЃЛ
ЃЈ4ЃЉИљОнвдЩЯЪЕбщПЩжЊЃКЂйNaHCO3ЙЬЬхгыбЮЫсЗДгІЪБЃЌЮТЖШНЕЕЭЃЌдвђЪЧNaHCO3ЙЬЬхШмгкЫЎЪБЮќШШЃЌNaHCO3гыбЮЫсЕФЗДгІвВЪЧЮќШШЗДгІЃЛЂкNa2CO3ЙЬЬхгыбЮЫсЗДгІЪБЃЌЮТЖШЩ§ИпЃЌдвђЪЧNa2CO3ЙЬЬхШмгкЫЎЪБЗХШШЃЌNa2CO3гыбЮЫсЕФЗДгІвВЪЧЗХШШЗДгІЃЌЙЪД№АИЮЊЃКЂйNaHCO3ЙЬЬхгыбЮЫсЗДгІЪБЃЌЮТЖШНЕЕЭЃЌдвђЪЧNaHCO3ЙЬЬхШмгкЫЎЪБЮќШШЃЌNaHCO3гыбЮЫсЕФЗДгІвВЪЧЮќШШЗДгІЃЛЂкNa2CO3ЙЬЬхгыбЮЫсЗДгІЪБЃЌЮТЖШЩ§ИпЃЌдвђЪЧNa2CO3ЙЬЬхШмгкЫЎЪБЗХШШЃЌNa2CO3гыбЮЫсЕФЗДгІвВЪЧЗХШШЗДгІЃЎ


 ПкЫуаФЫуЫйЫугІгУЬтЯЕСаД№АИ
ПкЫуаФЫуЫйЫугІгУЬтЯЕСаД№АИ ЭЌВНЭиеЙдФЖСЯЕСаД№АИ
ЭЌВНЭиеЙдФЖСЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЪЧ( )
A.габѕЦјВЮМгЕФЗДгІвЛЖЈЪЧШМЩе
B.ШМЩевЛЖЈвЊгабѕЦјВЮМг
C.ЧтЦјдкТШЦјжаШМЩеЃЌЛ№бцГЪТЬЩЋ
D.ШЮКЮЗЂЙтЗХШШЕФОчСвЕФЛЏбЇЗДгІЖМПЩвдНаШМЩе
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНЋПеЦјЛКТ§ЭЈЙ§ШчЭМЫљЪОзАжУКѓЃЌдкЪдЙмжаЪеМЏЕНЩйСПЯЁгаЦјЬхЁЃПеЦјдкЭЈЙ§aЁЋdзАжУЪБЃЌвРДЮГ§ШЅЕФЦјЬхЪЧ (ЁЁ ЁЁ)
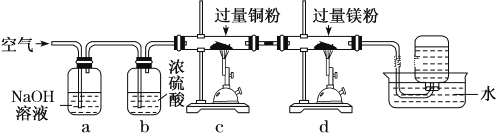
A. O2ЁЂN2ЁЂH2OЁЂCO2 B. CO2ЁЂH2OЁЂO2ЁЂN2
C. CO2ЁЂH2OЁЂN2ЁЂO2 D. N2ЁЂO2ЁЂCO2ЁЂH2O
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкNa2CO3КЭNaHCO3ЕФЫЕЗЈжаЃЌВЛе§ШЗЕФЪЧ
A. ОљЪєгкбЮ
B. бцЩЋЗДгІОљЮЊЛЦЩЋ
C. ПЩвдгУМгШШЕФЗНЗЈГ§ШЅNa2CO3ЙЬЬхжаЕФNaHCO3дгжЪ
D. ЮяжЪЕФСПЯрЭЌЕФСНжжЙЬЬхЗжБ№гызуСПбЮЫсЗДгІЃЌNa2CO3ВњЩњЕФЖўбѕЛЏЬМЖр
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮРЩњВПбЯСюНћжЙдкУцЗлЩњВњжаЬэМгЙ§бѕЛЏИЦ(CaO2)ЕШЪГЦЗЬэМгМСЁЃЙ§бѕЛЏИЦ(CaO2)ГЃгУзїЩБОњМСЁЂЗРИЏМСЃЌЪЧвЛжжАзЩЋЙЬЬхЃЌДјгаНсОЇЫЎЃЌЭЈГЃЛЙКЌгаCaOЁЃ
IЁЂжЦБИЙ§бѕЛЏИЦЁЃ
ФГЪЕбщаЁзщбЁгУШчЯТзАжУжЦБИЙ§бѕЛЏИЦЁЃвбжЊЛЏбЇЗДгІCa2ЃЋЃЋH2O2ЃЋ2NH3ЃЋxH2O===CaO2ЁЄxH2OЁ§ЃЋ2NH4+ЁЃдкМюадЛЗОГжажЦШЁCaO2ЁЄxH2OЕФзАжУШчЯТЭМЃК
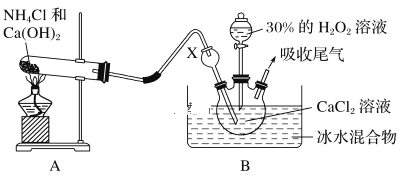
ЃЈ1ЃЉзАжУBжавЧЦїXЕФзїгУЪЧ_____________ЃЛЗДгІдкБљЫЎдЁжаНјааЕФдвђЪЧ_________________ЁЃ
ЃЈ2ЃЉЗДгІНсЪјКѓЃЌО________ЁЂ________ЁЂЕЭЮТКцИЩЛёЕУCaO2ЁЄxH2OЁЃ
IIЁЂКЌСПВтЖЈЁЃ
ЃЈ1ЃЉГЦШЁ13.52 gЙ§бѕЛЏИЦбљЦЗЃЌзЦШШЪБЗЂЩњШчЯТЗДгІЃК2[CaO2ЁЄxH2O]Ёњ2CaOЃЋO2ЁќЃЋ2xH2OЃЌЕУЕНO2дкБъзМзДПіЯТЬхЛ§ЮЊ672 mLЃЌИУбљЦЗжаCaO2ЕФЮяжЪЕФСПЮЊ____________ЁЃ
ЃЈ2ЃЉСэШЁЭЌвЛбљЦЗ13.52 gЃЌШмгкЪЪСПЯЁбЮЫсжаЃЌШЛКѓМгШызуСПЕФNa2CO3ШмвКЃЌНЋШмвКжаCa2ЃЋШЋВПзЊЛЏЮЊCaCO3ГСЕэЃЌЕУЕНИЩдяЕФCaCO3 7.0 gЁЃбљЦЗжадгжЪCaOЕФжЪСПЮЊ_____________ЃЛбљЦЗCaO2ЁЄxH2OжаЕФxжЕЮЊ____________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМзЛљБћЯЉЫсМзѕЅЪЧКЯГЩгаЛњВЃСЇЕФЕЅЬхЃЌЦфКЯГЩЗНЗЈжЎвЛШчЯТЃКCH3OCЁдCH+CH3OH+A ![]() CH2=C(CH3)COOCH3ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
CH2=C(CH3)COOCH3ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
A. вбжЊИУЗДгІЕФдзгРћгУТЪЮЊ100%ЃЌдђAЮЊCO2
B. CH3OHКЭИЪгЭЛЅЮЊЭЌЯЕЮя
C. CH3CЁдCHгыБћЯЉЕФаджЪЯрЫЦЃЌдђИУЮяжЪПЩвдЗЂЩњМгГЩЁЂбѕЛЏЗДгІ
D. ФмгыNaHCO3ЗДгІЕФCH2=C(CH3)COOCH3ЕФЭЌЗжвьЙЙЬхга9жж
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАбзуСПЪьЪЏЛвЗХШыеєСѓЫЎжаЃЌвЛЖЮЪБМфКѓДяЕНЦНКтЃКCa(OH)2(s)![]() Ca2+(aq)+2OH-(aq),ЯТСаа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
Ca2+(aq)+2OH-(aq),ЯТСаа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
A. ЯђШмвКжаМгШыЩйСПЕФNaOHЙЬЬхЃЌдђЦфжаЕФCa(OH)2ЕФЙЬЬхдіЖр
B. ЯђШмвКжаМгШыNa2CO3ШмвКЃЌдђЦфжаЕФCa(OH)2ЕФЙЬЬхдіЖр
C. КуЮТЯТЯђШмвКжаМгШыCaOЃЌШмвКЕФpHЩ§Ип
D. ИјШмвКМгШШЃЌШмвКЕФpHЩ§Ип
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПIЃЎГЃЮТЯТНЋ0.01 mol NH4ClКЭ0.002 mol NaOHШмгкЫЎХфГЩ1 LШмвКЁЃ
(1)ИУШмвКжаДцдкЕФЦНКтЬхЯЕгаЃЈгУРызгЗДгІЗНГЬЪНБэЪОЃЉ________
(2)ШмвКжаЙВга________ жжВЛЭЌЕФЮЂСЃЁЃ
(3)етаЉЮЂСЃжаХЈЖШЮЊ0.01 molЁЄLЃ1ЕФЪЧ_____ЃЌХЈЖШЮЊ0.002 molЁЄLЃ1ЕФЪЧ___ЁЃ
(4)______КЭ_______СНжжЮЂСЃЕФЮяжЪЕФСПжЎКЭБШOHЃЕФЮяжЪЕФСПЖр0.008 molЁЃ
IIЃЎ(5)дкДжжЦCuSO4ЁЄ5H2OОЇЬхжаГЃКЌгадгжЪFe2ЃЋЁЃ
ЂйдкЬсДПЪБЮЊСЫГ§ШЅFe2ЃЋЃЌГЃМгШыКЯЪЪбѕЛЏМСЃЌЪЙFe2ЃЋбѕЛЏЮЊFe3ЃЋЃЌЯТСаЮяжЪПЩВЩгУЕФЪЧ________ЁЃ
AЃЎKMnO4 BЃЎH2O2 CЃЎТШЫЎ DЃЎHNO3
ЂкШЛКѓдйМгШыЪЪЕБЮяжЪЕїећШмвКжСpHЃН4ЃЌЪЙFe3ЃЋзЊЛЏЮЊFe(OH)3ЃЌЕїећШмвКpHПЩбЁгУЯТСажаЕФ______ЁЃ
AЃЎNaOH BЃЎNH3ЁЄH2O CЃЎCuO DЃЎCu(OH)2
(6)МзЭЌбЇЛГвЩЕїећжСШмвКpHЃН4ЪЧЗёФмДяЕНГ§ШЅFe3ЃЋЖјВЛЫ№ЪЇCu2ЃЋЕФФПЕФЃЌввЭЌбЇШЯЮЊПЩвдЭЈЙ§МЦЫуШЗЖЈЃЌЫћВщдФгаЙизЪСЯЕУЕНШчЯТЪ§ОнЃЌГЃЮТЯТFe(OH)3ЕФШмЖШЛ§KspЃН1.0ЁС10Ѓ38ЃЌCu(OH)2ЕФШмЖШЛ§KspЃН3.0ЁС10Ѓ20ЃЌЭЈГЃШЯЮЊВаСєдкШмвКжаЕФРызгХЈЖШаЁгк1.0ЁС10Ѓ5 molЁЄLЃ1ЪБОЭШЯЮЊГСЕэЭъШЋЃЌЩшШмвКжаCuSO4ЕФХЈЖШЮЊ3.0 molЁЄLЃ1ЃЌдђCu(OH)2ПЊЪМГСЕэЪБШмвКЕФpHЮЊ________ЃЌFe3ЃЋЭъШЋГСЕэ[МДc(Fe3ЃЋ)Ём1.0ЁС10Ѓ5 molЁЄLЃ1]ЪБШмвКЕФpHЮЊ________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ1ЃЉвбжЊВнЫсЃЈH2C2O4ЃЉПЩЪЙH2SO4ЫсЛЏЕФKMnO4ШмвКЭЪЩЋЃЌЧыЛиД№вдЯТЮЪЬтЃК
ЂйЧыВЙШЋВЂХфЦНИУЗДгІЗНГЬЪНЃК
_____H2C2O4+___KMnO4+___H2SO4 Ёњ ___K2SO4+____ MnSO4+___ CO2Ёќ + ___H2O
ЂкдкИУЗДгІЛЙдВњЮяЮЊ________ЃЈаДЛЏбЇЪНЃЉ
ЃЈ2ЃЉФГШмвКжаПЩФмКЌгавдЯТРызгЃКNa+ЁЂK+ЁЂFe3+ЁЂCO32ЃЁЂSO42ЃЁЂClЃЃЌЯжНјааШчЯТЪЕбщЃК

ИљОнЪЕбщЯжЯѓЛиД№ЃК
ИУШмвКжавЛЖЈКЌгаЕФРызгЪЧ______________ЃЛвЛЖЈВЛКЌгаЕФРызгЪЧ____________ЃЛЮоЗЈШЗЖЈЕФРызгЪЧ____________________ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com