
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既不是氧化剂又不是还原剂等。下列反应与Br2 + SO2 + 2H2O H2SO4 + 2HBr相比较,水的作用不相同的是
A.2Na2O2 + 2H2O 4NaOH + O2↑ B.4Fe(OH)2 + O2 + 2H2O 4Fe(OH)3
C.2F2 + 2H2O 4HF + O2 D.C12 + H2O HC1 + HC1O
 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列叙述正确的是(相对原子量:H—1 C—12)
A.1 mol/L氯化铜溶液中的Cu2+数小于NA
B.标准状况下,22.4 L Cl2参加任何化学反应转移的电子数都是2NA
C.28 g聚乙烯含有的碳原子数为2NA
D.1 mol CH5+所含电子数为8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
将10.7g 氯化铵固体与足量熟石灰混合加热,使之充分反应。
(1)生成的氨气在标准状况下的体积是多少升?
(2)若将这些氨气溶于水配成500ml氨水,该氨水的物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表述与化学用语对应且正确的是
A. CO2的比例模型:
B. 溴乙烷的消去反应: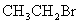

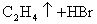
C. 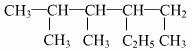 的名称:2,3—二甲基—4—乙基己烷
的名称:2,3—二甲基—4—乙基己烷
D. 乙酸乙酯的水解:
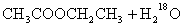


查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D之间的转化关系如图所示。下列说法正确的是
 A. 若A为Fe,D为氢气,则B一定为酸
A. 若A为Fe,D为氢气,则B一定为酸
B. 若A、D为化合物,B为水,则C一定是气体单质
C. 若A、B、C、D均为化合物,该反应一定属于复分解反应
D. 若A、B、C、D均为10电子微粒,且C是可使湿润的红色石蕊试纸变蓝的气体,则D常温下一定呈液态
查看答案和解析>>
科目:高中化学 来源: 题型:
I、实验室需要200mL 0.4 mol/L的碳酸钠溶液。
(1)需准确称量碳酸钠固体____________g。
(2)必须用到的仪器是(填写序号)_______________。
①100 mL量筒 ②烧杯 ③100 mL容量瓶 ④250 mL容量瓶 ⑤天平和砝码
⑥胶头滴管 ⑦玻璃棒
(3)若出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是____________。
A. 将已溶解的碳酸钠溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B. 将烧杯内的碳酸钠溶液向容量瓶内转移时,因操作不当使部分溶液溅出瓶外
C. 用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切
II、某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
(1)三次检测结果中第 _____①_____次检测结果不正确。
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子(提示:Ag2SO4微溶于水);
第一步:向溶液中滴加过量的______②______溶液(填化学式),其目的是检验CO32-并将其除去;发生反应的离子方程式为 ③ 。
第二步:加入过量的______④_______溶液(填化学式),其目的是______⑤______;
第三步:过滤,再向滤液中加入_____⑥_______溶液(填化学式),发生反应的离子方程式_____________________⑦____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
13gZn与100mL稀HCl恰好完全反应。求:
(1)标准状况下生成H2的体积;
(2)生成ZnCl2 的物质的量
(3)原稀HCl的物质的量浓度。
(4)用双线侨法表示该反应中电子转移的方向和数目
查看答案和解析>>
科目:高中化学 来源: 题型:
某含氯化合物A由两种短周期元素组成,常温下该物质为气态,测得该气体对空气的相对密度为3.0,A溶于水可得只含单一溶质B的弱酸性溶液,B溶液在放置过程中其酸性会增强。常温下,气体A与NH3反应生成离子晶体C、气体单质D和常见液体E,D为空气中含量最多的物质。气体A可用某一气体单质与潮湿的Na2CO3 反应制得,同时生成两种钠盐。请回答下列问题:
(1)气体A的化学式为 ,气体单质D对应元素在周期表中的位置为 。
(2)用化学方程式表示B溶液酸性增强的原因 。
(3)气体A与NH3反应的化学方程式为 ,该反应体现气体A具有 性。
(4)试写出制取气体A的化学方程式为 。
(5)设计实验探究离子晶体C的成分为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com