
| A. | 烧碱溶液与小苏打溶液反应:OH-+HCO3═H2O+CO2↑ | |
| B. | 氯水与烧碱溶液反应:2Al+2OH-+H2O═2AlO2-+2H2↑ | |
| C. | 氯化亚铁溶液中滴加氯水:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | 氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-═3Cl-+ClO-+H2O |
分析 A.不符合反应客观事实;
B.得失电子不守恒;
C.二者反应生成氯化亚铁;
D.电荷不守恒.
解答 解:A.烧碱溶液与小苏打溶液反应生成碳酸钠和水,离子方程式:OH-+HCO3═H2O+CO32-,故A错误;
B.铝与烧碱溶液反应,离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑,故B错误;
C.氯化亚铁溶液中滴加氯水,离子方程式:2Fe2++Cl2═2Fe3++2Cl-,故C正确;
D.氯气通入冷的氢氧化钠溶液中,离子方程式:Cl2+2OH-═Cl-+ClO-+H2O,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 28g氮气所含有的原子数目为NA | |
| B. | 16g O2中所含的氧原子数为NA | |
| C. | 标准状况下,22.4L水中含有NA个水分子 | |
| D. | 标准状况下,22.4L氯化氢所含的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃、101.3kPa时,11.2L H2中含有的原子数为NA | |
| B. | 39g Na2O2与足量水充分反应时转移的电子数为0.5NA | |
| C. | 17 g羟基与17 g氨气所含电子数均为10NA | |
| D. | 1mol/L Na2SO4溶液中离子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3、NH4+、NH-的电子数相等,化学性质也相同 | |
| B. | 一定温度下液氨中c(NH4+)•c(NH2-)是一个常数 | |
| C. | 液氨的电离达到平衡时c(NH3)≠c(NH4+)=c(NH2-) | |
| D. | 加入其他物质,c(NH4+)/c(NH2-)可能不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
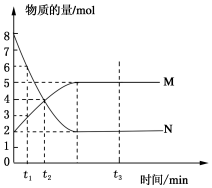 一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝是地壳中含量最多的金属元素 | |
| B. | 在常温下,铝不能与浓硫酸反应 | |
| C. | 铝是一种比较活泼的金属 | |
| D. | 在化学反应中,铝容易失去电子,是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 起始物质的量(mol) | 3 | 2 | 0 |
| 2s末物质的量浓度(mol/L) | 0.9 | 0.8 | 0.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com