
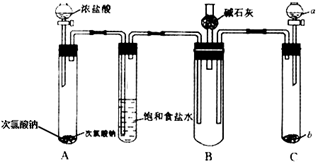
分析 由装置可知,A中浓盐酸与NaClO反应生成氯气,饱和食盐水可除去HCl,C中利用Zn与稀硫酸反应生成氢气(或浓硫酸与亚硫酸盐反应生成二氧化硫或浓氨水与碱石灰反应生成氨气等),在B中A、C中产生的气体发生反应,B中碱石灰可吸收尾气,防止污染环境,以此来解答.
解答 解:(1)A中有分液漏斗,可利用液差法检验气密性,则实验前检查A部分装置的气密性的方法为用止水夹夹住A导管,关闭分液漏斗活塞,向分液漏斗中加水,打开分液漏斗活塞,试管中液面与分液漏斗液面产生一段高度差,且维持一段时间不变.说明气密性良好,
故答案为:用止水夹夹住A导管,关闭分液漏斗活塞,向分液漏斗中加水,打开分液漏斗活塞,试管中液面与分液漏斗液面产生一段高度差,且维持一段时间不变.说明气密性良好;
(2)碱石灰的作用是吸收多余Cl2防止污染大气;NaClO在反应中作氧化剂,可选KClO3(或K2CrO7、KMnO4)代替,也能达到同样的目的,
故答案为:吸收多余Cl2防止污染大气;KClO3;
(3)实验过程中可能发生爆炸,因H2、Cl2混合见光爆炸,则C中气体为氢气,a中为稀硫酸,b中为Zn(或Fe),
故答案为:稀硫酸、Zn(或Fe);H2、Cl2混合见光爆炸;
(4)在B中将会看到白烟生成,则C中生成的气体为氨气,a、b分别为浓氨水、碱石灰(CaO,NaOH均可),生成白烟的化学方程式为3Cl2+8NH3═6NH4Cl+N2,
故答案为:浓氨水、碱石灰(CaO,NaOH均可);3Cl2+8NH3═6NH4Cl+N2.
点评 本题考查性质实验方案的设计,为高频考点,把握物质的性质、实验装置的作用、实验技能等为解答的关键,侧重分析与实验能力的考查,注意C中气体的判断具有较高的开放性,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C02的电子式::$\underset{\stackrel{…}{O}}{…}$:$\underset{\stackrel{…}{C}}{…}$:$\underset{\stackrel{…}{O}}{…}$ | B. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | ||
| C. | 乙烯的比例模型 | D. | 铝离子结构示意图: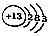 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2、CH4、N2等均是造成温室效应的气体 | |
| B. | 石油是混合物,其分馏产品汽油是纯净物 | |
| C. | 二氧化硫可以使酸性高锰酸钾溶液褪色,体现二氧化硫的漂白性 | |
| D. | 石油催化裂化和裂解可以获得更多的汽油和乙烯、丙烯等气态短链烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸中滴加氨水:H++OH-═H2O | |
| B. | 用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ | |
| C. | 铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | 将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性强弱:H2SiO3<H3PO4<H2SO4<HClO4 | |
| B. | 碱性强弱:KOH>NaOH>Mg(OH)2>Al(OH)3 | |
| C. | 熔点:Li<Na<K | |
| D. | 热稳定性:HF>HCl>H2S>PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 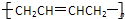 | B. | 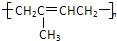 | C. | 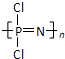 | D. | 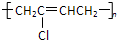 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不宜用瓷坩埚灼烧氢氧化钠或碳酸钠 | |
| B. | 使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大 | |
| C. | 分液操作时,由于分液漏斗下端已沾满下层液体,故上层液体要从上口倒出 | |
| D. | 用托盘天平称量11.74g氯化钠晶体 | |
| E. | 用结晶法分离硝酸钾和氯化钠的混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com