
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3 NaHCO3 CH3COONa NaF | |
| B. | NaHCO3 Na2CO3 CH3COONa NaF | |
| C. | NaF CH3COONa Na2CO3 NaHCO3 | |
| D. | NaF CH3COONa NaHCO3Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入KHSO4溶液 | B. | 将水加热到100℃,使pH=6 | ||
| C. | 向水中加入Na3PO4溶液 | D. | 向水中加入ZnSO4固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa2O2固体中含阴离子个数为2NA | |
| B. | 1molSiO2中含Si-O的数目为2NA | |
| C. | 标准状况下,22.4L乙炔中含π键数为2NA | |
| D. | 1molNaHCO3晶体中阳离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MnCl2溶液中常含有Cu2+,可添加难溶电解质MnS除去:Cu2++S2-=CuS↓ | |
| B. | 盛放NaOH溶液的试剂瓶不能用玻璃塞是因为:SiO2+2OH-=SiO32-+H2O | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 向氨水中滴入少量饱和氯化铁溶液制各Fe(OH)3胶体:Fe3++3NH3•H2O?Fe(OH)3(胶体)+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
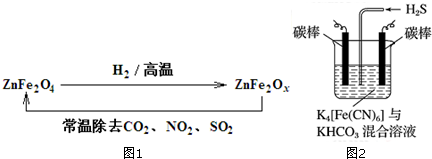
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com