
分析 a方案一:(1)滴加足量沉淀剂,把溶液中HCO3-、CO32-完全转化为沉淀,关键是该沉淀剂能够与碳酸氢根离子反应生成沉淀;
(2)可以直接向原溶液中加入氢氧化钡溶液,根据反应现象判断HCO3-、CO32-是否沉淀完全;
(3)根据过滤操作的方法判断需要使用的仪器名称;
(4)洗涤沉淀的操作为:向漏斗中的沉淀中加入蒸馏水,直到淹没沉淀,静置让水自行留下,重复2-3次;
(5)沉淀未干燥充分就称量,则称量值偏大,由于在质量相等的条件下碳酸氢钠产生的沉淀大于碳酸钠产生的沉淀,据此判断对测定结果的影响;
b方案二:(1)碳酸钠、碳酸氢钠的混合液显碱性,应该用碱式滴定管量取;
(2)酚酞的变色范围是8.2~10.0,反应结束时溶液由红色突变为无色,据此判断滴定终点;反应方程式为:H++CO32-=HCO3-;
(3)根据反应H++CO32-=HCO3-计算出50 mL样品溶液中含有的碳酸钠的物质的量,然后计算出250mL样品溶液中含有的碳酸钠的物质的量,再根据m=nM计算出碳酸钠的质量,最后根据质量分数的表达式计算出样品中碳酸钠的质量分数.
解答 解:a方案一:(1)A.CaCl2溶液只能与碳酸根反应转化为碳酸根沉淀,故A错误;
B.MgSO4溶液与HCO3-、CO32-均不反应,故B错误;
C.NaCl溶液与HCO3-、CO32-都不反应,故C错误;
D.Ba(OH)2溶液与HCO3-、CO32-都发生反应生成碳酸钡沉淀,故D正确;
故答案为:D;
(2)要证明HCO3-、CO32-已完全沉淀,则可以继续滴加氢氧化钡溶液,即正确的实验操作方法为:静置、澄清,在澄清溶液中继续加Ba(OH)2溶液,不浑浊,则HCO3-、CO32-已沉淀完全,反之,未沉淀完全,
故答案为:静置、澄清,在澄清溶液中继续加Ba(OH)2溶液,不浑浊,则HCO3-、CO32-已沉淀完全,反之,未沉淀完全;
(3)过滤操作所需要的玻璃仪器有:烧杯、玻璃棒、普通漏斗,
故答案为:烧杯、玻璃棒、普通漏斗;
(4)洗涤沉淀的操作为:向漏斗中的沉淀中加入蒸馏水,直到淹没沉淀,静置让水自行留下,重复2-3次,
故答案为:向漏斗中的沉淀中加入蒸馏水,直到淹没沉淀,静置让水自行留下,重复2-3次;
(5)如果此步中,沉淀未干燥充分就称量,则称量值偏大,由于在质量相等的条件下碳酸氢钠产生的沉淀大于碳酸钠产生的沉淀,所以如果称量值偏大,则碳酸氢钠的质量偏大,则碳酸钠的含量偏小,故答案为:偏小;
b方案二:(1)溶液显碱性,因此应该用碱式滴定管量取,故答案为:碱式滴定管;
(2)酚酞的变色范围是8.2~10.0,所以判断滴定终点的依据是由红色突变为无色,且30s不恢复,发生的离子方程式为:H++CO32-=HCO3-,
故答案为:由红色突变为无色,且30s不恢复;H++CO32-=HCO3-;
(3)反应达到终点时,发生的离子方程式为:H++CO32-=HCO3-,
则根据消耗盐酸的体积可知20.00ml可知,消耗碳酸钠的物质的量为:0.2000 mol/L×0.02000L=0.004mol,
则原混合物中碳酸钠的物质的量为:0.004mol×$\frac{250ml}{25ml}$=0.04mol,质量为:0.04mol×106g/mol=4.24g,
所以碳酸钠质量分数为:$\frac{4.24g}{5.1g}$×100%=83.14%,
故答案为:83.14.
点评 本题考查碳酸钠和碳酸氢钠混合物中碳酸钠含量测定的实验方案设计与评价,题目难度中等,明确化学实验基本操作方法及碳酸钠、碳酸氢钠的性质为解答此题关键,试题充分考查了学生的分析、理解能力及化学实验、化学计算能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH+HCl═NaCl+H2O | B. | CuO+H2SO4═CuSO4+H2O | ||
| C. | Zn+2H+═Zn2++H2↑ | D. | CaO+H2O═Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
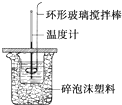 利用如图所示装置测定中和热的实验步骤如下:
利用如图所示装置测定中和热的实验步骤如下:| 温度 实验次数 | 超始温度t1℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | / |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的性质与用途: 磺胺类药物能抑制细菌合成核酸--治疗肺炎、脑膜炎、尿路感染、呼吸道感染 酸能与碱中和-----胃酸过多的病人服用含氢氧化钠的药物 | |
| B. | 保护环境: 控制“白色污染”--减少和控制使用所有塑料制品 防止水的污染--提倡使用无磷洗衣粉 | |
| C. | 基本安全常识: 饮用假酒中毒--由甲醇引起 食用假盐中毒--由亚硝酸钠引起 | |
| D. | 生活中的一些做法: 除去衣服上的油污--可用汽油洗涤 使煤燃烧更旺--可增大煤与空气接触面积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
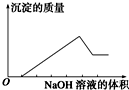 某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤HCO3-、⑥Cl-、⑦OH-.向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是( )
某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤HCO3-、⑥Cl-、⑦OH-.向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是( )| A. | ①②⑤ | B. | ①③④ | C. | ②⑥⑦ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com