
【题目】下列有关描述不正确的是
A.新制饱和氯水和浓硝酸光照下均会有气体产生,其成分中都有氧气
B.灼烧NaOH固体时不能使用瓷坩埚,因为瓷坩埚中的SiO2能与NaOH反应
C.钠在空气和氯气中燃烧,火焰皆呈黄色,但生成固体颜色不同
D.浓硫酸具有较强酸性,能与Cu反应生成H2
【答案】D
【解析】
A、新制饱和氯水中含有HClO,HClO不稳定,在光照条件下会发生分解:2HClO![]() 2HCl+O2↑,浓硝酸在光照条件下会发生分解:4HNO3
2HCl+O2↑,浓硝酸在光照条件下会发生分解:4HNO3![]() 4NO2↑+2H2O+O2↑,故A不符合题意;
4NO2↑+2H2O+O2↑,故A不符合题意;
B、因为瓷坩埚中的SiO2能与NaOH反应,故灼烧NaOH固体时不能使用瓷坩埚,一般使用铁坩埚加热熔融NaOH,故B不符合题意;
C、钠在空气燃烧,生成物为淡黄色固体过氧化钠,钠在氯气中燃烧,生成物为白色固体氯化钠,因钠元素的焰色反应为黄色,故钠在空气和氯气中燃烧,火焰皆呈黄色,故C不符合题意;
D、浓硫酸具有强酸性和强氧化性,但在常温下不与Cu反应,在加热条件下,与Cu反应生成物为硫酸铜、二氧化硫、水,不会生成H2,故D符合题意。


科目:高中化学 来源: 题型:
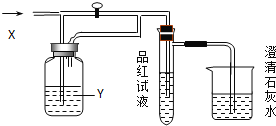
【题目】向如图装置中缓慢地通入气体X,若关闭活塞,则品红溶液无变化,而澄清石灰水变浑浊;若打开活塞,则品红溶液褪色,加热后又恢复红色.据此判断气体X和洗气瓶内溶液Y分别可能是 ( )
A | B | C | D | |
X | SO2 | H2S | CO2 | Cl2 |
Y | 饱和NaHCO3 | 浓硫酸 | Na2SO3 | NaHCO3 |
A.A正确B.B正确C.C正确D.D正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将pH=l的盐酸平均分成2份,l份加适量水,另1份加入与该盐酸物质的量浓度相同的适量NaOH溶液后,pH都升高了1,则加入的水与NaOH溶液的体积比为_____。
(2)在25℃下,将pH=3的硫酸溶液和pH=10的NaOH溶液混合,若要使混合后溶液的pH=7,则硫酸溶液和NaOH溶液的体积比约为___
(3)在250C时,有pH为a的盐酸和pH为b的NaOH溶液,取Va L该盐酸,同该NaOH溶液中和,需Vb LNaOH溶液。填空:
①若a + b = 14,则Va∶Vb =_____(填数字)。
②若a + b = 13,则Va∶Vb =_______(填数字)。
③若a + b >14,则Va∶Vb =______(填表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国有广阔的海岸线,建设发展海洋经济、海水的综合利用大有可为。空气吹出法工艺,是目前“海水提漠”的最主要方法之一。其工艺流程如图所示,试回答下列问题:
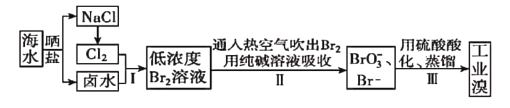
(1)以上步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是_____。
(2)步骤②通入热空气或水蒸气吹出![]() ,利用了溴的___。
,利用了溴的___。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)流程Ⅱ中涉及的离子反应方程式如下,请在下面横线内填入适当的化学计量数:
![]() ____
____
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:____。
(5)流程Ⅲ蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用足量的一氧化碳还原4.64 g某金属氧化物,把生成的二氧化碳全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0 g,则此金属氧化物是下列中的( )
A. 氧化铜 B. 氧化铁 C. 四氧化三铁 D. 二氧化锰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
(1)ClO2的制备:
已知:SO2+NaClO3+H2SO4=2ClO2↑+2NaHSO4
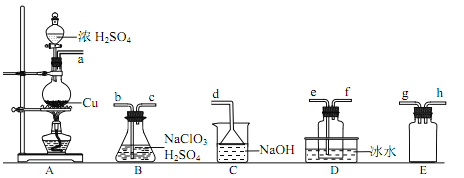
①装置A中反应的化学方程式为________________。
②欲收集干燥的ClO2,选择上图中的装置,其连接顺序为A→_______、_______、_______→C(按气流方向)。
③装置D的作用是_______________。
(2)ClO2与Na2S的反应
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究Ⅰ中反应的产物。

操作步骤 | 实验现象 | 结论 |
取少量I中溶液于试管甲中,滴加品红溶液和盐酸 | 品红始终不褪色 | ①无___生成 |
另取少量I中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ②____________ | 有SO42生成 |
③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管丙内_________ | 有白色沉淀生成 | 有Cl生成 |
④ClO2与Na2S反应的离子方程式为___________。用于处理含硫废水时,ClO2相对于Cl2的优点是______________(任写一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无论是干重还是鲜重,组成水生动物、人体细胞的元素中含量最多的四种元素是
A.O、N、H、CaB.O、Ca、P、Mg
C.C、O、N、HD.C、Fe、Ca、P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知钠、铁都能与水反应,下列叙述不正确的是( )
A.它们反应的难易程度不同B.它们反应的产物不完全相同
C.都需在高温条件下进行D.反应类型都是置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p轨道的电子数等于次外层的电子总数,B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7∶8,E与B的质量比为1∶1。根据以上条件,回答下列问题:
(1)画出C的原子结构示意图:________。
(2)写出D原子的外围电子排布式:________。
(3)写出A元素单质在B中完全燃烧的化学方程式:______________。
(4)指出E元素在元素周期表中的位置:____________。
(5)比较A、B、C三种元素的第一电离能的大小顺序:________________(按由大到小的顺序排列,用元素符号表示)。
(6)比较元素D和E的电负性的相对大小:__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com